题目内容
17.下列叙述正确的是( )| A. | 与28 g CO具有相同分子数的CO2的质量一定是44 g | |
| B. | 与V L CO具有相同分子数的CO2的体积一定是V L | |
| C. | 等质量的H2S和PH3含有相同的原子数 | |
| D. | 同温同压下,相同体积的物质,其物质的量一定相等 |
分析 A、根据m=nM=$\frac{N}{{N}_{A}}$M计算;
B、气体体积受温度和压强的影响;
C、设二者的质量均为34g,则n(H2S)=$\frac{34g}{34g/mol}$=1mol,n(PH3)=$\frac{34g}{34g/mol}$=1mol;
D、同温同压下,相同体积的气体物质,其物质的量一定相等.
解答 解:A、28gCO的物质的量是1mol,与28gCO具有相同分子数的CO2的物质的量也是1mol,1mol二氧化碳的质量是44g,故A正确;
B、气体体积受温度和压强的影响,温度和压强不同,气体摩尔体积不同,所以与VLCO具有相同分子数的CO2的体积不一定是VL,故B错误;
C、1molH2S中含有3mol原子,1molPH3中含有4mol原子,原子数不同,故C错误;
D、同温同压下,相同体积的气体物质,其物质的量一定相等,而固体和液体就不一定相等,故D错误;
故选A.
点评 本题考查物质的量的有关计算,明确二者的摩尔质量相同、质量与物质的量的关系、物质的构成等即可解答,难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
7.如图装置用来检验氯气的部分性质,下列说法不正确的是( )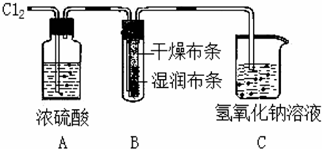

| A. | 装置A的作用是除去氯气中的水蒸汽 | |
| B. | 装置B的现象是干燥处布条褪色,湿润处布条不褪色 | |
| C. | 装置C中发生反应为Cl2+2NaOH=NaCl+NaClO+H2O | |
| D. | 该实验必须在通风橱中进行 |
8.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 22.4 L CO和CO2的混合气体中所含的碳原子数一定是NA | |
| B. | 标准状况下,22.4L H2O含有的分子数为NA | |
| C. | 46 g金属钠在氯气中充分燃烧生成NaCl,反应中转移电子数为2NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
9.下列有关热化学方程式的叙述正确的是( )
| A. | 已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 | |
| B. | 含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为: NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l)△H=-57.4kJ•mol-1 | |
| C. | 已知2C(s)+2O2(g)=2CO2(g)△H1; 2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2[ | |
| D. | 已知2H2(g)+O2(g)=2H2O(l);△H=-571.6 kJ•mol-1,则氢气的燃烧热为285.8 kJ•mol-1 |