题目内容
【题目】钴酸锂电池是目前用量最大的钾离子电池,用它作电源按下图装置进行电解。通电后。a电极上一直有气泡产生;d电极附近先出现白色沉淀(CuCl),后白色沉淀逐渐转变成橙黄色沉淀(CuOH)。下列有关叙述正确的是( )

A. 已知钴酸锂电池放电时总反应为Li1-xCoO2+LixC6=LiCoO2+6C,则Li1-xCoO2作负极,失电子
B. 当外电路中转移0.2mol电子时,电极b处有2.24LCl2生成
C. 电极d为阴极,电解开始时的电极反应式为Cu+Cl--e-=CuCl
D. 所着电解的进行,U形管1中发生了如下转化CuCl+OH-=CuOH+Cl-
【答案】D
【解析】A、LixC6中C为负价,根据电池总反应,LixC6作负极,则Li1-xCoO2为正极,得到电子,故A错误;B、没有说明是否是标准状况,因此无法直接计算氯气的体积,故B错误;C、a电极一直有气泡产生,又因为a极的材料为铜棒,因此a极为阴极,即d电极为阳极,电极反应式为Cu+Cl--e-=CuCl,故C错误;D、d电极先产生白色沉淀CuCl,白色沉淀逐渐转变成橙黄色沉淀CuOH,发生的反应是CuCl+OH-=CuOH+Cl-,故D正确。

 名校课堂系列答案
名校课堂系列答案【题目】如图所示的过程是目前直接利用太阳能的研究热点。人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。
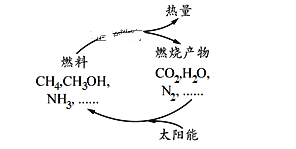
(1)在上图构想的物质和能量循环中太阳能最终转化为____________能。
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)![]() 2CH3OH(g)+3O2(g)。
2CH3OH(g)+3O2(g)。
一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
①用CH3OH表示0~3 min内该反应的平均反应速率为______________________。
②能说明该反应已达到平衡状态的是_______________。
a.v正(H2O)=2v逆(CO2) b.n(CH3OH) :n(O2)=2 :3
c.容器内密度保持不变 d.容器内压强保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的____极(填“正”或“负”),通入氧气的一极的电极反应式为_______________。