题目内容
科学研究往往建立在合理的假设之上.下面是两个对照实验:

(1)提出问题,实验一中的CO2能灭火,而实验二中的CO2为何能“点火”?
(2)对实验二提出的解释:
CO2被Na2O2吸收.可能生成Na2CO3;棉花被点燃,说明上述反应
(3)现有一定量含有Na2O杂质的Na2O2试样.请从下图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体,6mol/L盐酸和蒸馏水).
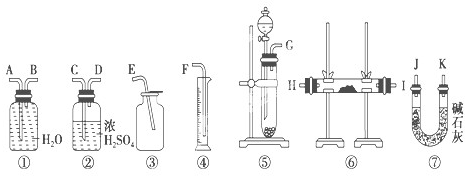
请填写下列空白:
(1)写出实验中Na2O2发生反应的化学方程式:
(2)应选用的装置是

(1)提出问题,实验一中的CO2能灭火,而实验二中的CO2为何能“点火”?
(2)对实验二提出的解释:
CO2被Na2O2吸收.可能生成Na2CO3;棉花被点燃,说明上述反应
是放热反应
是放热反应
;棉花燃烧剧烈,说明上述反应生成了氧气
生成了氧气
.(3)现有一定量含有Na2O杂质的Na2O2试样.请从下图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体,6mol/L盐酸和蒸馏水).

请填写下列空白:
(1)写出实验中Na2O2发生反应的化学方程式:
2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH
2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH
,(2)应选用的装置是
⑤②①④
⑤②①④
(只要求写出图中装置的标号).分析:(2)根据过氧化钠与二氧化碳的反应是放热反应,反应后生成的氧气使棉花燃烧剧烈进行分析;
(3)(1)氧化钠和过氧化钠均能和水反应;
(2)根据氧化钠和过氧化钠与水反应的区别:过氧化钠和水反应生成氢氧化钠溶液的同时,还会生成氧气,可以用排水量气法测定氧气的体积,进而确定过氧化钠的量及其百分含量;
(3)(1)氧化钠和过氧化钠均能和水反应;
(2)根据氧化钠和过氧化钠与水反应的区别:过氧化钠和水反应生成氢氧化钠溶液的同时,还会生成氧气,可以用排水量气法测定氧气的体积,进而确定过氧化钠的量及其百分含量;
解答:解:(3)由于过氧化钠与二氧化碳的反应是放热反应,使棉花燃烧;反应后生成的氧气使棉花燃烧剧烈,
故答案为:是放热反应;生成了氧气;
(3)(1)氧化钠和过氧化钠均能和水反应,方程式为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH;
(2)实验的原理是:过氧化钠和水反应生成氢氧化钠溶液的同时,还会生成氧气,但氧气中会有水蒸气,要用浓硫酸吸水,然后可以用排水量气法测定氧体的体积,进而确定过氧化钠的量及其百分含量,故可选择的装置为⑤①④即可,
故答案为:⑤②①④;
故答案为:是放热反应;生成了氧气;
(3)(1)氧化钠和过氧化钠均能和水反应,方程式为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH;
(2)实验的原理是:过氧化钠和水反应生成氢氧化钠溶液的同时,还会生成氧气,但氧气中会有水蒸气,要用浓硫酸吸水,然后可以用排水量气法测定氧体的体积,进而确定过氧化钠的量及其百分含量,故可选择的装置为⑤①④即可,
故答案为:⑤②①④;
点评:本题主要考查学生金属钠的氧化物和过氧化物的性质以及用排水量气法测定气体的体积的方法,难度不大.

练习册系列答案
相关题目



