题目内容
13.下列四种物质能与氢气发生加成反应的是( )| A. |  | B. | CH4 | C. | CuO | D. | C2H5OH |
分析 根据能发生加成反应的物质有:烯烃、炔烃、苯及其同系物、酚、醛、酮等.
解答 解:A、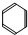 能与氢气发生加成反应,生成环己烷,故A正确;
能与氢气发生加成反应,生成环己烷,故A正确;
B、CH4中不含有不饱和键,不能与氢气发生加成反应,故B错误;
C、CuO能与氢气发生氧化还原反应,但不属于加成反应,故C错误;
D、C2H5OH中不含有不饱和键,不能与氢气发生加成反应,故D错误;
故选:A.
点评 本题考查有机物的结构与性质,注意把握有机物中的官能团,题目难度不大.

练习册系列答案
相关题目
16.下列根据物质组成推断相关信息,正确的是( )
| A. | 过二硫酸钾的化学式为K2S2O8,其中硫元素为+6价 | |
| B. | KMnO4和K2MnO4中原子团组成相同,其化学性质相同 | |
| C. | 有机物的分子式、结构简式、实验式都不相同 | |
| D. | 摩尔质量相同的物质,其化学式一定相同 |
4.能正确表示下列反应的离子方程式是( )
| A. | 少量CO2通入苯酚钠溶液中:C6H5O-+CO2+H2O═C6H5OH+HCO3- | |
| B. | NaHCO3溶液中加入稀HCl:CO32-+2H+═CO2↑+H2O | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+2H2O | |
| D. | 醋酸溶液中加入少量CaCO3固体:CaCO3+2H+═Ca2++H2O+CO2↑ |
1.下列各组离子既能与镁粉反应,又能大量共存,且其溶液为无色溶液的是( )
| A. | Ca2+、Cl-、$MnO_4^-$、Na+ | B. | K+、Cl-、$SO_4^{2-}$、H+ | ||
| C. | OH-、Na+、Al3+、I- | D. | H+、Cl-、Ba2+、Ag+ |
8.下列反应中,硝酸既表现酸性,又表现氧化性的是( )
| A. | Fe(OH)2跟稀硝酸反应 | B. | Fe2O3跟稀硝酸反应 | ||
| C. | CuO跟稀硝酸反应 | D. | Al(OH)3跟稀硝酸反应 |
2.2011年3月11日日本地震损坏核电站设备,引起核泄漏.钚是核工业重要原料,原子核内质子数为94,有多种同位素如钚-238、钚-242、钚-244等,下列关于钚-238说法错误的是( )
| A. | 钚是f 区元素 | B. | 核外电子数238 | C. | 核内中子数 144 | D. | 钚是锕系元素 |
19.短周期元素X、Y、W、R的原子序数依次增大,元素X是形成化合物种类最多的元素,Y、R同主族,R原子的最外层电子数是内层电子总数的一半,W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )
| A. | W元素是硅元素 | |
| B. | 气态氢化物的稳定性:Y<R | |
| C. | X、W、Y的最高价氧化物的水化物酸性强弱顺序是X<Y<W | |
| D. | X、Y、W、R的原子半径由大到小的顺序为R>W>X>Y |
5. 甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.
甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.
已知:
①2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ•mol-1
②CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g)△H2=-36kJ•mol-1
③CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+216kJ•mol-1
(1)氢气的燃烧热为△H=-285.8kJ•mol-1,写出甲烷不完全燃烧生成一氧化碳和液态水的热化学方程式:CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(l)△H=-607.6kJ•mol-1.
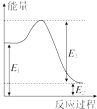
(2)现有1mol由H2O(g)与O2组成的混合气体,且O2的体积分数为x,将此混合气体与足量CH4充分反应.当x=0.75时,反应②与③放出(或吸收)的总能量为0.若②反应过程中能量转化过程如图所示,下列有关说法中正确的是C.
A.E1=36kJ B.E2=36kJ
C.E1-E2=36kJ D.E3-E1=36kJ
(3)工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g)═CH3OH(g)△H1(CO结构式为C≡O).又知某些化学键的键能(断开1mol化学键时所需要的最低能量)数值如下表:
则△H1=-116kJ•mol-1,在相应的反应条件下,将1mol CO(g)与足量H2混合充分反应后,放出或吸收的热量<△H1.(用>,<或=填空)
 甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.
甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.已知:
①2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ•mol-1
②CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g)△H2=-36kJ•mol-1
③CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+216kJ•mol-1
(1)氢气的燃烧热为△H=-285.8kJ•mol-1,写出甲烷不完全燃烧生成一氧化碳和液态水的热化学方程式:CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(l)△H=-607.6kJ•mol-1.
(2)现有1mol由H2O(g)与O2组成的混合气体,且O2的体积分数为x,将此混合气体与足量CH4充分反应.当x=0.75时,反应②与③放出(或吸收)的总能量为0.若②反应过程中能量转化过程如图所示,下列有关说法中正确的是C.
A.E1=36kJ B.E2=36kJ
C.E1-E2=36kJ D.E3-E1=36kJ
(3)工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g)═CH3OH(g)△H1(CO结构式为C≡O).又知某些化学键的键能(断开1mol化学键时所需要的最低能量)数值如下表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ•mol-1) | 348 | 413 | 436 | 358 | 1072 | 463 |
 现有反应:A、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
现有反应:A、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑