题目内容
5.标准状况下,CO的摩尔质量是( )| A. | 28 | B. | 28g | C. | 28g/mol | D. | 22.4L/mol |
分析 CO的相对分子质量为28,在数值上等于摩尔质量,注意单位为g/mol,以此解答.
解答 解:CO的相对分子质量为28,摩尔质量在数值上等于相等分子质量,单位为g/mol,则CO的摩尔质量是28g/mol,
故选C.
点评 本题考查物质的量的相关知识,为高频考点,侧重于摩尔质量的考查,注意把握相关概念以及公式的理解和运用,难度不大.

练习册系列答案
相关题目
15.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上一般可采用下列反应合成甲醇:
CO(g)+2H2(g)═CH3OH(g)△H
(1)化学平衡常数(K)的表达式为$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$.
(2)下表所列数据是该反应在不同温度下的化学平衡常数(K)
由表中数据判断△H<0 (填“>”、“=”或“<”).
(3)某温度下,将6mol CO和4.4mol H2充入2L的密闭容器中,10min该反应达到平衡,测得c(CO)=2.4mol•L-1,则用H2表示的10min内该反应的反应速率为0.12mol•L-1•min-1,此时的温度为300℃(从上表中选择),H2转化率=54.5%.
(4)判断该可逆反应达到化学平衡状态的标志是③④⑥(填序号).
①单位时间内,消耗2mol H2,同时生成1molCH3OH
②混合气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④CO、H2、CH3OH的浓度均不再变化
⑤CO、H2、CH3OH的分子数目比为1:2:1
⑥混合气体的总压强不再变化.
CO(g)+2H2(g)═CH3OH(g)△H
(1)化学平衡常数(K)的表达式为$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$.
(2)下表所列数据是该反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.04 | 0.25 | 0.012 |
(3)某温度下,将6mol CO和4.4mol H2充入2L的密闭容器中,10min该反应达到平衡,测得c(CO)=2.4mol•L-1,则用H2表示的10min内该反应的反应速率为0.12mol•L-1•min-1,此时的温度为300℃(从上表中选择),H2转化率=54.5%.
(4)判断该可逆反应达到化学平衡状态的标志是③④⑥(填序号).
①单位时间内,消耗2mol H2,同时生成1molCH3OH
②混合气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④CO、H2、CH3OH的浓度均不再变化
⑤CO、H2、CH3OH的分子数目比为1:2:1
⑥混合气体的总压强不再变化.
13.在PH=1的透明溶液中可大量共存的是( )
| A. | Cu2+、SO42-、K+、Na+ | B. | Na+、Cl-、HSO3-、K+ | ||
| C. | MnSO4-、CO32-、Na+、K+ | D. | Fe3+、SO42-、S2-、Na+ |
10.铜与稀硝酸反应,不能生成的物质是( )
| A. | Cu(NO3)2 | B. | NO | C. | H2O | D. | H2 |
17.现有100mL 0.1mol/L NaCl 溶液,从中取出10mL,此10mL NaCl 溶液的物质的量浓度为( )
| A. | 0.1mol/L | B. | 0.01mol/L | C. | 0.001mol/L | D. | 无法确定 |
14.下列事故处理方法正确的是( )
| A. | 实验室钠着火时,立即用水灭火 | |
| B. | 不慎洒出的酒精在桌上着火时,应立即用大量水扑灭 | |
| C. | 浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 | |
| D. | 浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤 |
15.下列说法中正确的是( )
| A. | 将硫酸钡放入水中不能导电,所以硫酸钡是非电解质 | |
| B. | SO3的水溶液能导电,所以SO3是电解质 | |
| C. | 乙醇在水溶液和熔融状态下均不能导电,所以乙醇属于非电解质 | |
| D. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
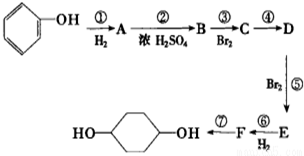 已知实验室由
已知实验室由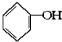 合成
合成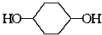 的反应流程如图(部分试剂和反应条件已略去) (X代表卤素原子,R代表烃基)请回答下列问题:
的反应流程如图(部分试剂和反应条件已略去) (X代表卤素原子,R代表烃基)请回答下列问题: 、D
、D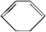 .
.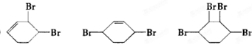 (其中一种).(写出一种即可)
(其中一种).(写出一种即可)