题目内容
16.下列反应的离子方程式错误的是( )| A. | NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-═NH3↑+H2O | |
| B. | 向碳酸氢钙溶液中滴入少量的NaOH溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 在Ba(OH)2溶液中加入过量NH4HSO4溶液:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 草酸和氨水反应:HOOC-COOH+2NH3•H2O═C2O42-+2NH4++2H2O |
分析 A.氢氧化钠过量,铵根离子和碳酸氢根离子都参与反应;
B.氢氧化钠少量,二者反应生成碳酸钙沉淀、碳酸氢钠和水;
C.硫酸氢铵过量,离子方程式按照氢氧化钡的化学式书写;
D.草酸与氨水反应生成醋酸铵和水,草酸需要保留化学式.
解答 解:A.碳酸氢啊与过量的氢氧化钠反应生成碳酸钠、一水合氨和水,正确的离子方程式为:NH4++HCO3-+2OH-═CO32-+H2O+NH3•H2O,故A错误;
B.向碳酸氢钙溶液中滴入少量的NaOH溶液,反应生成碳酸钙、碳酸氢钠和水,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,故B正确;
C.在Ba(OH)2溶液中加入过量NH4HSO4溶液,二者反应的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C正确;
D.草酸和氨水反应生成醋酸铵和水,反应的离子方程式为HOOC-COOH+2NH3•H2O═C2O42-+2NH4++2H2O,故D正确;
故选A.
点评 本题考查了离子方程式的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
6.要增大锌与盐酸反应的速率,所采取的下列措施无效的是( )
| A. | 增大盐酸的浓度 | B. | 提高反应的温度 | C. | 用锌粉代替锌片 | D. | 用纯锌代替粗锌 |
7.常温下,将浓度为0.1mol﹒L-1HCOOH的溶液加水不断稀释,下列各量始终保持增大的是( )
| A. | c(H+) | B. | Ka(HCOOH) | C. | $\frac{c(HCO{O}^{-})}{c({H}^{+})}$ | D. | $\frac{c({H}^{+})}{c(HCOOH)}$ |
4.钠在空气中长期露置,最终变成( )
| A. | Na2O | B. | Na2O2 | C. | Na2CO3 | D. | NaOH |
1.下列说法不正确的是( )
| A. | 我国最早使用的合金是由铜锌合金制成的青铜器 | |
| B. | 储氢合金是一类能大量吸收H2,并与H2结合成金属氢化物的材料 | |
| C. | 一般汽车配件中的发动机使用的是密度小、强度大且耐腐蚀的铝合金材料 | |
| D. | 钛合金,形状记忆合金,耐热合金以及储氢合金都属于新型合金 |
8.下列有关说法正确的是( )
| A. | 气体的摩尔体积即标准状况下单位物质的量气体的体积 | |
| B. | 温度压强一定的情况下,气体的体积决定于气体的物质的量多少和分子本身的大小 | |
| C. | 配制物质的量浓度的溶液,定容时俯视,配得溶液浓度偏大 | |
| D. | 电解18g水,两极生成的气体体积比约为2:1,质量比2:16 |
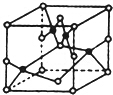 A、B、C、D、E、F六种元素的原子序数依次增大.已知:F的原子序数为29,其余均为短周 期主族元素;E原子价电子(外围电子)排布式为 msnmpn-1;D原子的最外层电子数为偶数;A、C原子 的P轨道上都有两个未成对电子.请回答下列问题:
A、B、C、D、E、F六种元素的原子序数依次增大.已知:F的原子序数为29,其余均为短周 期主族元素;E原子价电子(外围电子)排布式为 msnmpn-1;D原子的最外层电子数为偶数;A、C原子 的P轨道上都有两个未成对电子.请回答下列问题: