��Ŀ����
����Ŀ�����淴Ӧ2NO2![]() 2NO��O2���ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
2NO��O2���ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
�ٵ�λʱ��������nmolO2��ͬʱ����2nmolNO2
�ڵ�λʱ��������nmolO2��ͬʱ����2nmolNO
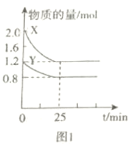
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
�ܻ���������ɫ���ٸı��״̬
���ܱպ��������£������ܶȲ���
���ܱպ��������£�����ƽ����Է�����������
A.�٢ۢܢ�B.�ڢ�C.�٢ܢ�D.�٢ڢܢ�
���𰸡�C
��������
����λʱ��������nmolO2��ͬʱ����2nmolNO2��������(O2)=![]() ����(NO2) =����(O2)���������淴Ӧ������ȣ�˵���Ѵ�ƽ�⣬�����ϣ�
����(NO2) =����(O2)���������淴Ӧ������ȣ�˵���Ѵ�ƽ�⣬�����ϣ�
���κ�ʱ������nmolO2��ͬʱ����2nmolNO���������ϣ�
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬��δָ�����ĸ���������ʣ��˴����ܵó� ������(O2)=![]() ����(NO2)�������Ľ��ۣ��������ϣ�
����(NO2)�������Ľ��ۣ��������ϣ�
������������ɫ���ٸı��״̬����NO2Ũ�Ȳ��ٱ仯�������ϣ�
���ܱպ��������£���Ϊ���������غ㣬�������ܶ�ʼ�ղ��䣬�������ϣ�
���ܱպ��������£���Ϊ���������غ㣬����������ʵ����淴Ӧ���仯��������ƽ����Է��������ᷢ���仯��������������ƽ�⣬�����ϣ�
��ѡC��