��Ŀ����
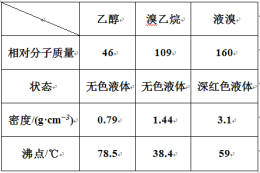
����Ŀ����ҵ�Ƶõĵ�������AlN����Ʒ�г���������Al4C3��Al2O3��C�����ʡ�ijͬѧ�������ʵ��ֱ�ⶨ��������AlN����Ʒ��AlN��Al4C3����������������NH3��ǿ������Һ�е��ܽ⣩��
��1��ʵ��ԭ����
��Al4C3�����ᷴӦ������CH4��
��AIN����ǿ�������Σ�����ǿ�����ɰ�������д��AlN��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��__________________________________________________________________
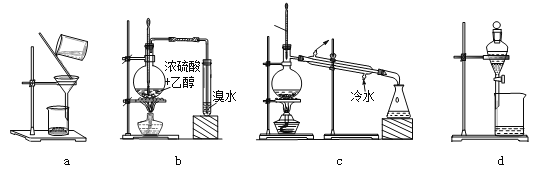
��2��ʵ��װ�ã���ͼ��ʾ��������Ϊ��ʽ�ζ��ܸ�װ��

����װ�ú�����Ӧ���еIJ�����_____________________________________ ��
��3��ʵ����̣��Ƶ�װ��D�ij�ʼ����Ϊy g����ȡx g AlN��Ʒ����װ��B��ƿ�У���װ���м�����ӦҩƷ����������װ�ã���ȡ�����ܵij�ʼ����Ϊa mL(����װ������Һ����ƽ)��
�������Ȳ���Al4C3�����������й����ݣ���K1��K2��K3���������IJ����ǹرջ���_______������______��
������ѹ�ܣ����������������Ӱ����_______���ƫ����ƫС������Ӱ�족����
����������Һ�治�ٷ����仯��˵����Ӧ�Ѿ���������ȡ����֮ǰ��Ӧ�������ܽ��еIJ���Ϊ ______________________________________ �����������е�Һ������Ҳ����������е�Һ�棬������������_________���ƫ����ƫС������Ӱ�족����
�ܼ�¼�ζ��ܵĶ���Ϊb mL����֪����ʵ�������µ�����Ħ�����ΪVm L�� mol��1������Al4C3����������Ϊ___________���ÿ��ܺ�a��b��x��y��Vm�Ĵ���ʽ��ʾ����
�ݲ���AlN�������������ݣ����ȹرջ���K1������K3��ͨ����Һ©���������NaOH��Һ����װ��Bƿ�����ʳ�ַ�Ӧ����Ӧ��ɺ�___________________________����ò�Ӧ���еIJ����������Ƶ�װ��D������Ϊz g��
���𰸡�AlN+NaOH+H2O=NaAlO2+NH3�� ���װ�õ������� K2��K3 K1 ƫ�� ���������ܸ߶ȣ�ʹ��������Һ����ƽ ƫС ![]() ��K2��ͨ��һ��ʱ�����
��K2��ͨ��һ��ʱ�����
��������
������һ���ۺ��⣬��Ҫ������ʵ���Լ���ѧ��Ӧ����ѧ������������Ҫͨ���������ɵ��������������Ʒ�Ĵ��ȣ��ݴ��������Ѷ�һ�㡣
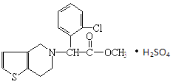
��1��![]() �е���Ԫ����+3�۵ģ�����ڼ��Ի����л�ת��Ϊ
�е���Ԫ����+3�۵ģ�����ڼ��Ի����л�ת��Ϊ![]() �����������Ϣ��֪����һ�ֲ����ǰ������ݴ�д������ʽ���ɣ�
�����������Ϣ��֪����һ�ֲ����ǰ������ݴ�д������ʽ���ɣ�![]() ��
��
��2���ڽ����漰�������ʵ��ʱ����װ��������һ��Ҫ�ȼ���������ٿ�ʼʵ�飬��������ʵ����������ʵ��ʧ�ܣ�
��3���ٸ������⣬��Ҫ֪��![]() ����������������Ҫ���
����������������Ҫ���![]() �����ᷴӦ���ɵ�
�����ᷴӦ���ɵ�![]() ������������Ҫʹ��װ��A�е������ܣ��������Ҫ�ȴ�K1���ر�K2��K3�������ɵĴ�
������������Ҫʹ��װ��A�е������ܣ��������Ҫ�ȴ�K1���ر�K2��K3�������ɵĴ�![]() �����������У�
������������
�ڷ�Һ©���ϵĺ�ѹ����ƽ��ѹǿ�����ã�����ѹ�ܣ�����B�е���Һ�ὫB�еĿ������ϡ��������ܣ�����������������ƫ��
���ڶ�ȡ����ǰһ��Ҫ�ȵ��������ܸ߶ȣ�ʹ��������Һ����ƽ�����Dz���������ʱ�Ļ���Ҫ������������Һ������Ҳ����������е�Һ�棬Ҳ����˵�Ҳ��ѹǿ�����в��ִ���������δ������������ܣ����²���������ƫС��
��ʵ���в����ļ������һ����![]() mL����ʵ��������Ϊ
mL����ʵ��������Ϊ![]() mol���飬�ɷ���ʽ��֪
mol���飬�ɷ���ʽ��֪![]() ��
��![]() �Ļ�ѧ������֮��Ϊ3:1����ԭ��Ʒ����
�Ļ�ѧ������֮��Ϊ3:1����ԭ��Ʒ����![]() mol
mol ![]() ��
��![]() ��Ħ������Ϊ144g/mol�����ԭ��Ʒ����
��Ħ������Ϊ144g/mol�����ԭ��Ʒ����![]() g
g![]() ����
����![]() ����������Ϊ
����������Ϊ![]() �������Ϊ
�������Ϊ![]() ��
��
��K2���������ڣ���Ӧ�������Ի�����������������װ��B�ڣ����ǿ��Դ�K2����ӿ����ã�ͨ�������װ��B�ڵİ������ϡ���װ��D�У�ȷ�����еİ�������D���գ��������Ҫ�����ǣ���K2��ͨ��һ��ʱ��Ŀ�����

 ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д� С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д�����Ŀ��KMnO4��ʵ���ҡ������ѧ�о�����ҵ�������й㷺��Ӧ�á���֪һ���Ʊ�KMnO4��ʵ�����̡�ԭ��������������£�

ԭ������ӦI��3MnO2+KClO3+6KOH![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
��Ӧ��3K2MnO4+2CO2=2KMnO4+MnO2��+2K2CO3
(ī��ɫ) (�Ϻ�ɫ)
��֪��25�����ʵ��ܽ��g/100gˮ
K2CO3 | KHCO3 | KMnO4 |
111 | 33.7 | 6.34 |
(1)����ڵĸ���Ӧ�����������������ɣ��÷�Ӧ�Ļ�ѧ����ʽΪ___________��
(2)�������CO2______(��ܡ�������)������ԭ����_____________��
(3)�����п�ѭ�����õ�������Ҫ��_________(д��ѧʽ)��
(4)���Ա������к������ʵ�ѭ�����ã�������0.3mol MnO2���õ���ƷKMnO4������Ϊ________g��ijͬѧ��ʵ���еõ������Ʒ��������������ֵ���ų��������أ��Ӳ���߷��������ܵ�ԭ����_______________��
(5)�����Ƶζ�������������ش��Ȳ������£�
��.��ȡ1.5800g������ز�Ʒ�����100mL��Һ
��.ȷ��ȡ����0.5360g�Ѻ�ɵ�Na2C2O4������������ͬ�Ľྻ��ƿ�У��ֱ������������ˮʹ���ܽ⣬�ټ������������ữ��
��.��ƿ����Һ���ȵ�75��80�棬������I�����Ƶĸ��������Һ�ζ����յ㡣��¼ʵ���������
ʵ����� | V1(�ζ�ǰ����/mL) | V2(�ζ������/mL) | (V2 -V1)/mL |
1 | 2.65 | 22.67 | 20.02 |
2 | 2.60 | 23.02 | 20.42 |
3 | 2.60 | 22.58 | 19.98 |
��֪��2MnO4��+ 5C2O42��+16H+ =2Mn/span>2++ 10CO2��+ 8H2O����KMnO4�Ĵ���Ϊ__________(������λ��Ч����)�����ζ����ӵζ��ܶ���������KMnO4�Ĵ��Ƚ�___(�ƫ�ߡ���ƫ�͡�����Ӱ�족)��