题目内容
14.由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去).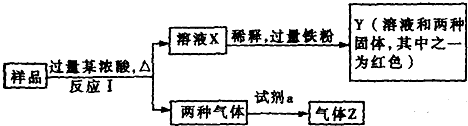
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2后无明显变化,说明样品中不可能含有的物质是Al(写化学式).
(2)Z可能为一种或两种气体.
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O.
②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是NO、CO2.
(3)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是Cu2+、Fe3+、H+(写离子符号).
(4)取Y中的溶液,调节pH约为7,加入淀粉-KI溶液和H2O2溶液,溶液呈蓝色并有红褐色沉淀生成,当消耗2mol I-时,共转移3mol电子,该反应的离子方程式是2Fe2++4I-+3H2O2=2Fe(OH)3↓+2I2.
分析 (1)根据金属铝可以和酸反应生成可溶性的铝盐,该铝盐可以和过量氢氧化钠反应生成偏铝酸盐,此盐可以和二氧化碳反应;
(2)①二氧化硫可以和饱和碳酸氢钠反应生成二氧化碳;
②一氧化氮不溶于水而二氧化碳能溶于水中;
(3)氯气能将亚铁离子氧化为三价铁离子;
(4)双氧水具有氧化性,能将还原性的离子碘离子、亚铁离子氧化.
解答 解:(1)金属铝可以和酸反应生成可溶性的铝盐,该铝盐可以和过量氢氧化钠反应生成偏铝酸盐,偏铝酸盐中通入二氧化碳反应可以获得氢氧化铝,故样品中不含有金属铝,故答案为:Al;
(2)①二氧化硫可以和饱和碳酸氢钠反应生成二氧化碳,所以反应Ⅰ获得的是二氧化硫和二氧化碳的混合气体,Z是二氧化碳,即C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O;
②二氧化氮可以和水反应生成一氧化氮气体,所以反应Ⅰ是焦炭和浓硝酸的反应,Z中两种气体是NO、CO2,故答案为:NO、CO2;
(3)Fe2O3、Fe、CuO、C均可以和浓酸反应,除了生成气体以外还有Cu2+、Fe2+、Fe3+、H+,通入过量的Cl2,并不断搅拌,充分反应后,氯气能将亚铁离子氧化为三价铁离子,过量的铁能将铜离子还原,此时存在的离子有Cu2+、Fe3+、H+,故答案为:Cu2+、Fe3+、H+;
(4)双氧水具有氧化性,能将还原性的离子碘离子、亚铁离子氧化,原理方程式为:2Fe2++4I-+3H2O2=2Fe(OH)3↓+2I2,
故答案为:2Fe2++4I-+3H2O2=2Fe(OH)3↓+2I2.
点评 本题主要考查的是无机推断,是一道物质的检验题目,可以根据所学知识进行回答,以实验流程的形式考查,增加了难度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列反应的离子方程式正确的是( )
| A. | AgOH溶于氨水:AgOH+2NH3•H2O=[Ag(NH3)2]++OHˉ+2H2O | |
| B. | Na2C2O4水解:C2O42-+2H2O=H2C2O4+2OH- | |
| C. | 向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- | |
| D. | 向酸性KMnO4溶液中通入SO2:2MnO4-+5SO2+4OH-=2Mn2++5SO42-+2H2O |
5.下列各组试剂中,能用溴水加以鉴别的是( )
| A. | CH4与C3H8 | B. | 苯与己烯 | C. | 己烷与苯 | D. | 苯与甲苯 |
3.设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 已知白磷(P4)为正四面体形,12.4 g白磷中则含有共价键数为0.4 NA | |
| B. | 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$ Fe3O4+4H2反应中,当5.6 g Fe全部转化为Fe3O4时,则有0.3 NA电子发生转移 | |
| C. | 在0.1 mol/L碳酸钠溶液中Na+总数等于0.2 NA | |
| D. | 电解精炼铜时,当电路中转移NA个电子时,阴极增重32g |
4.下列有关叙述中正确的是( )
| A. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| B. | 葡萄糖可以制乙醇,两者都能与金属钠反应 | |
| C. | 明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视 | |
| D. | 合成纤维和光导纤维都是有机高分子化合物 |
 已知A、B、C、D四种短周期主族元素位于同一周期,且它们的核电荷数依次增大.A原子,C原子的L能层中,都有两个未成对的电子,C、E同主族.F、G都是第四周期元素,F原子核外有4个未成对电子,G原子除最外能层只有1个电子外,其余各能层均为全充满.根据以上信息填空:
已知A、B、C、D四种短周期主族元素位于同一周期,且它们的核电荷数依次增大.A原子,C原子的L能层中,都有两个未成对的电子,C、E同主族.F、G都是第四周期元素,F原子核外有4个未成对电子,G原子除最外能层只有1个电子外,其余各能层均为全充满.根据以上信息填空: ,
, .
.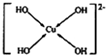 (需要用箭头指出配位键).
(需要用箭头指出配位键).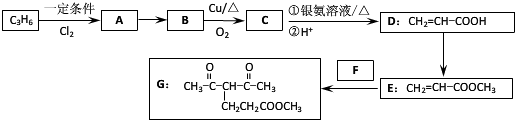
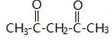 .
.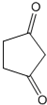 +CH2=CH-NO2$\stackrel{一定条件}{→}$
+CH2=CH-NO2$\stackrel{一定条件}{→}$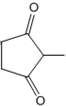 CH2CH2NO2
CH2CH2NO2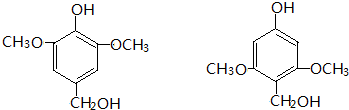 .
.
 回答下列问题:
回答下列问题: .
. .
.