题目内容
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,通入水蒸气,并加热,就可以完成高温下“Fe与水蒸气的反应实验”。
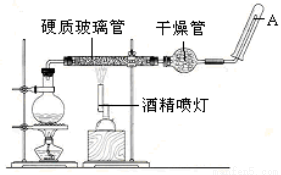
请回答该实验中的问题。
(1)写出该反应的反应方程式: 。
(2)实验前必须对整套装置进行气密性检查,操作方法是 。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 。
(4)酒精灯和酒精喷灯点燃的顺序是先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯;原因是 。
(5)干燥管中盛装是的物质是 。
(6)试管中收集气体是H2 ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行 ,
这一操作的目的是 。
(1)3Fe+4H2O(g)  Fe3O4+4H2↑;(2)将玻璃管口A处没入水中,加热烧瓶底部,如果能够观察到没入水中的玻璃管口有气泡产生,且停止加热后,玻璃管内能倒吸形成一段不回落的稳定水柱,则表明该套装置气密性良好。(3)为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气;防止爆沸。(4)防止先点燃酒精喷灯所导致的Fe与O2的反应。(5)无水硫酸铜(等干燥剂)。(6)验纯;防止点燃时,因氢气中含有氧气而爆炸。
Fe3O4+4H2↑;(2)将玻璃管口A处没入水中,加热烧瓶底部,如果能够观察到没入水中的玻璃管口有气泡产生,且停止加热后,玻璃管内能倒吸形成一段不回落的稳定水柱,则表明该套装置气密性良好。(3)为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气;防止爆沸。(4)防止先点燃酒精喷灯所导致的Fe与O2的反应。(5)无水硫酸铜(等干燥剂)。(6)验纯;防止点燃时,因氢气中含有氧气而爆炸。
【解析】
试题分析:(1)铁和水蒸气反应,铁的化合价升高,铁作还原剂,水中氢的化合价降低,水作氧化剂,反应的化学方程式为:3Fe+4H2O(g) Fe3O4+4H2;(2)将玻璃管口A处没入水中,加热烧瓶底部,如果能够观察到没入水中的玻璃管口有气泡产生,且停止加热后,玻璃管内能倒吸形成一段不回落的稳定水柱,则表明该套装置气密性良好;(3)因为反应物为水蒸气与铁,所以这里加热的目的就是为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气,碎瓷片的作用是防止爆沸。(4)点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,排掉硬质玻璃管内空气,为Fe与水蒸气的反应实验提供持续不断的水蒸气;(5)铁与水蒸气反应生成四氧化三铁和氢气,无水硫酸铜、碱石灰和氢气不反应,所以可用无水硫酸铜、碱石灰干燥剂除去反应产生的H2中的水蒸气;(6)铁与水蒸气反应生成四氧化三铁和氢气,氢气的爆炸极限是4.0%~75.6%,就是说当氢气的含量在上述范围内的话就会引起爆炸,因此,点燃之前要检验纯度。
Fe3O4+4H2;(2)将玻璃管口A处没入水中,加热烧瓶底部,如果能够观察到没入水中的玻璃管口有气泡产生,且停止加热后,玻璃管内能倒吸形成一段不回落的稳定水柱,则表明该套装置气密性良好;(3)因为反应物为水蒸气与铁,所以这里加热的目的就是为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气,碎瓷片的作用是防止爆沸。(4)点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,排掉硬质玻璃管内空气,为Fe与水蒸气的反应实验提供持续不断的水蒸气;(5)铁与水蒸气反应生成四氧化三铁和氢气,无水硫酸铜、碱石灰和氢气不反应,所以可用无水硫酸铜、碱石灰干燥剂除去反应产生的H2中的水蒸气;(6)铁与水蒸气反应生成四氧化三铁和氢气,氢气的爆炸极限是4.0%~75.6%,就是说当氢气的含量在上述范围内的话就会引起爆炸,因此,点燃之前要检验纯度。
考点:铁及其化合物的性质实验

 字词句段篇系列答案
字词句段篇系列答案