题目内容
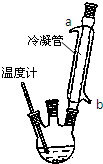
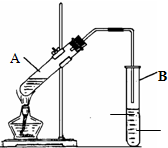 实验室利用如图所示装置制取乙酸乙酯.请回答:
实验室利用如图所示装置制取乙酸乙酯.请回答:(1)试管A中盛放的试剂为
乙醇
乙醇
、乙酸和浓硫酸,它们之间发生反应生成乙酸乙酯的化学方程式为CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
| 浓硫酸 |
| △ |
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
.| 浓硫酸 |
| △ |
(2)加热一段时间后,可观察到B试管中液面
上
上
(填“上”或“下”)有无色油状液体生成.若分离该液体混合物,需要用到的玻璃仪器是分液漏斗
分液漏斗
,这种方法叫做分液
分液
.(3)B试管中的导管不伸入液面下的原因是
①
①
(填序号).①防止溶液倒吸 ②避免反应过快
①乙酸可使紫色石蕊试液变红,说明乙酸具有
酸
酸
性.写出乙酸与碳酸钠溶液反应的离子方程式2CH3COOH+CO32-=2CH3COO?+H2O+CO2↑
2CH3COOH+CO32-=2CH3COO?+H2O+CO2↑
.分析:(1)实验室用乙醇在乙酸在浓硫酸作用下加热制备乙酸乙酯;
(2)乙酸乙酯密度比水小,不溶于饱和碳酸钠溶液,可用分液的方法分离;
(3)由于混合物中含有乙醇和乙酸,易溶于水,易生产倒吸,乙酸具有酸性,酸性比碳酸强.
(2)乙酸乙酯密度比水小,不溶于饱和碳酸钠溶液,可用分液的方法分离;
(3)由于混合物中含有乙醇和乙酸,易溶于水,易生产倒吸,乙酸具有酸性,酸性比碳酸强.
解答:解:(1)实验室用乙醇在乙酸在浓硫酸作用下加热制备乙酸乙酯,反应的化学方程式为CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,为可逆反应,
故答案为:乙醇;CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;
(2)乙酸乙酯密度比水小,在溶液的上层,不溶于饱和碳酸钠溶液,可用分液的方法分离,用分液漏斗分离混合物,
故答案为:上;分液漏斗;分液;
(3)由于混合物中含有乙醇和乙酸,易溶于水,易生产倒吸,实验时导管不能插入到液面以下,乙酸可使紫色石蕊试液变红,说明乙酸具有酸性,酸性比碳酸强,
与碳酸钠反应的离子方程式为2CH3COOH+CO32-=2CH3COO?+H2O+CO2↑,
故答案为:①;酸;2CH3COOH+CO32-=2CH3COO?+H2O+CO2↑.
| 浓硫酸 |
| △ |
故答案为:乙醇;CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
(2)乙酸乙酯密度比水小,在溶液的上层,不溶于饱和碳酸钠溶液,可用分液的方法分离,用分液漏斗分离混合物,
故答案为:上;分液漏斗;分液;
(3)由于混合物中含有乙醇和乙酸,易溶于水,易生产倒吸,实验时导管不能插入到液面以下,乙酸可使紫色石蕊试液变红,说明乙酸具有酸性,酸性比碳酸强,
与碳酸钠反应的离子方程式为2CH3COOH+CO32-=2CH3COO?+H2O+CO2↑,
故答案为:①;酸;2CH3COOH+CO32-=2CH3COO?+H2O+CO2↑.
点评:本题考查乙酸乙酯的制备,题目难度不大,本题注意把握乙酸乙酯的实验药品、仪器以及实验操作的注意事项等问题,学习中注意相关基础知识的积累.

练习册系列答案
相关题目
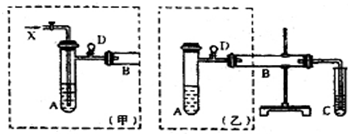
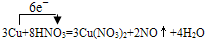
 CO↑+H2O)
CO↑+H2O)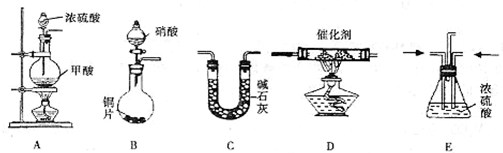
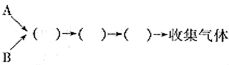
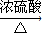 CO↑+H2O)
CO↑+H2O)