题目内容
为探究锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是( )
| A.加入NH4HSO4固体,v(H2)不变 |
| B.加入Na2SO4固体,v(H2)减小 |
| C.加入CH3COONa固体,v(H2)减小 |
| D.滴加少量CuSO4溶液,v(H2)减小 |
A.加入NH4HSO4固体,电离出氢离子,氢离子浓度增大,v(H2)增大,故A错误;
B.加入Na2SO4固体,氢离子浓度不变,v(H2)不变,故B错误;
C.加入CH3COONa固体,反应生成醋酸,氢离子浓度减小,则v(H2)减小,故C正确;
D.滴加少量CuSO4溶液,构成原电池,v(H2)增大,故D错误;
故选:C.
B.加入Na2SO4固体,氢离子浓度不变,v(H2)不变,故B错误;
C.加入CH3COONa固体,反应生成醋酸,氢离子浓度减小,则v(H2)减小,故C正确;
D.滴加少量CuSO4溶液,构成原电池,v(H2)增大,故D错误;
故选:C.

练习册系列答案
相关题目

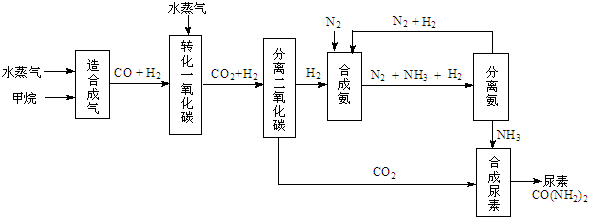
 CO(g)+3H2(g);△H>0
CO(g)+3H2(g);△H>0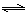 H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下: