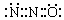题目内容
下列说法正确的是
| A.活化分子碰撞即发生化学反应 |
| B.升高温度会加快反应速率,原因是增加了活化分子的碰撞次数 |
| C.某一反应的活化分子百分数是个定值 |
| D.活化分子的碰撞不一定是有效碰撞 |
D
试题分析:活化分子碰撞需要有合适的取向时才能发生化学反应,故活化分子的碰撞不一定是有效碰撞,A错D对;升高温度会加快反应速率,最主要的原因是增加了活化分子的百分数,B错;活化分子的百分数受温度、催化剂等影响,C错误。
点评:碰撞理论、活化分子是理解影响反应速率的因素的基础。理论性较强,难得偏大。

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目