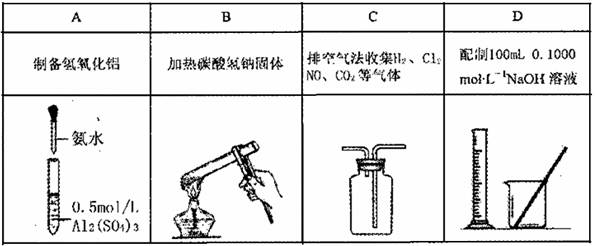
��Ŀ����
�±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��û�ѧ����ش��������⣺

(1)�ܢݢ�ԭ�Ӱ뾶��С�����˳��Ϊ(��Ԫ�ط��ű�ʾ) ��
�ڢۢߵ���ۺ����������������ǿ��˳����(�û�ѧʽ��ʾ) ��
(2)д��������ijЩԪ�ع��ɵļȺ����Ӽ����ֺ����Թ��ۼ��Ļ�����ĵ���ʽ(д��һ�ּ���) ��
(3)��֪������1 g�ٵ����ڢܵ�����ȼ�������ȶ���Һ̬����ʱ�ų�142.9 kJ���������ʾ�ٵ���ȼ�յ��Ȼ�ѧ����ʽΪ ��
(4)�٢��γɵ���Ļ�������ܵ�����KOH���������Һʱ���γ�ԭ��أ����и����ĵ缫��ӦΪ ��
(5)�ɱ���Ԫ�آ٢ۢܢޢ����γɵij�������X��Y��Z��M��N�ɷ������·�Ӧ��

��X��Һ��Y��Һ��Ӧ�����ӷ���ʽΪ ��
��N���ĵ��������õķ����� ��
��M��Һ�����ԣ�ԭ����(�����ӷ���ʽ����) ��

(1)�ܢݢ�ԭ�Ӱ뾶��С�����˳��Ϊ(��Ԫ�ط��ű�ʾ) ��
�ڢۢߵ���ۺ����������������ǿ��˳����(�û�ѧʽ��ʾ) ��
(2)д��������ijЩԪ�ع��ɵļȺ����Ӽ����ֺ����Թ��ۼ��Ļ�����ĵ���ʽ(д��һ�ּ���) ��
(3)��֪������1 g�ٵ����ڢܵ�����ȼ�������ȶ���Һ̬����ʱ�ų�142.9 kJ���������ʾ�ٵ���ȼ�յ��Ȼ�ѧ����ʽΪ ��
(4)�٢��γɵ���Ļ�������ܵ�����KOH���������Һʱ���γ�ԭ��أ����и����ĵ缫��ӦΪ ��
(5)�ɱ���Ԫ�آ٢ۢܢޢ����γɵij�������X��Y��Z��M��N�ɷ������·�Ӧ��

��X��Һ��Y��Һ��Ӧ�����ӷ���ʽΪ ��
��N���ĵ��������õķ����� ��
��M��Һ�����ԣ�ԭ����(�����ӷ���ʽ����) ��
(1)O��Al��Na��H2SiO3��H2CO3��HNO3
(2)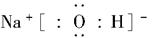 (�𰸺�������)(3)H2(g)��1/2O2(g)=H2O(l)��H����285.8 kJ��mol��1
(�𰸺�������)(3)H2(g)��1/2O2(g)=H2O(l)��H����285.8 kJ��mol��1
(4)CH4��8e����10OH��=CO32-��7H2O
(5)��Al3����3NH3��H2O=Al(OH)3����3NH4+
�ڵ�ⷨ ��NH4+��H2O NH3��H2O��H��
NH3��H2O��H��
(2)
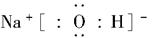 (�𰸺�������)(3)H2(g)��1/2O2(g)=H2O(l)��H����285.8 kJ��mol��1
(�𰸺�������)(3)H2(g)��1/2O2(g)=H2O(l)��H����285.8 kJ��mol��1(4)CH4��8e����10OH��=CO32-��7H2O
(5)��Al3����3NH3��H2O=Al(OH)3����3NH4+
�ڵ�ⷨ ��NH4+��H2O
 NH3��H2O��H��
NH3��H2O��H��(1)�ܢݢֱ�ΪO��Na��Al�����Ӳ���Խ�࣬��뾶Խ����λ��ͬһ���ڣ���˵������İ뾶����С��ͬ���壬����������Ӧˮ��������ԣ��������¼�����ͬ���ڣ����Դ���������ǿ��(2)���Ӽ�Ӧ�����ڻ��ý���Ԫ����ǽ���Ԫ��(NH4Cl����)֮�䣬���Թ��ۼ������ڲ�ͬ�ַǽ���Ԫ��֮�䡣(4)CH4��O2��Ӧ����CO2��CO2��KOH������Ӧ����CO32-�����Ը�����Ӧ�IJ���ΪCO32-��(5)MΪ�����ǽ���Ԫ�ص��Σ���ӦΪ��Σ���ΪAlԪ�أ���ͼ������֪��X��Y��Ӧ��ӦΪAl3���백ˮ�ķ�Ӧ��AlΪ���ý�������Ӧ���õ�ⷨ��á������Һ����������ΪNH4+ˮ�⡣

��ϰ��ϵ�д�
�����Ŀ