题目内容
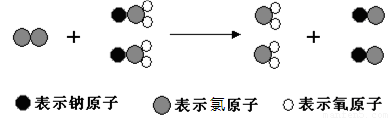
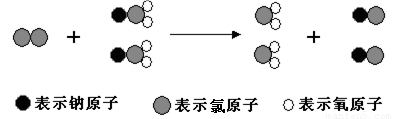
ClO2是新一代饮用水的消毒剂,许多发达国家的自来水厂采用ClO2代替Cl2来进行自来水消毒.我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图:
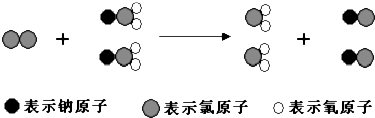
下列有关该反应的叙述中正确的是( )

下列有关该反应的叙述中正确的是( )
| A、该反应是复分解反应 | B、NaClO2和ClO2中Cl的化合价相同 | C、该反应涉及的物质中只含有极性键和离子键 | D、该反应的化学方程式为Cl2+2NaClO2═2ClO2+2NaCl |
分析:A、复分解反应是化合物与化合物反应生成化合物与化合物的反应;
B、根据化合价规则来确定元素的化合价;
C、大多数金属元素和非金属元素之间形成的化学键是离子键,不同的非金属元素之间形成的化学键是极性键,相同的非金属元素之间形成的化学键是非极性键;
D、由不同小球代表的原子及反应的微观过程来分析,书写反应方程式.
B、根据化合价规则来确定元素的化合价;
C、大多数金属元素和非金属元素之间形成的化学键是离子键,不同的非金属元素之间形成的化学键是极性键,相同的非金属元素之间形成的化学键是非极性键;
D、由不同小球代表的原子及反应的微观过程来分析,书写反应方程式.
解答:解:A、由不同的小球代表的原子可知,反应物为氯气和NaClO2,氯气为单质,则该反应一定不是复分解反应,故A错误;
B、根据化合价规则,NaClO2和ClO2中Cl的化合价分别是+3价和+4价,化合价不一样,故B错误;
C、该反应涉及的物质含有Cl2、NaClO2、ClO2、NaCl,其中NaClO2、NaCl中均含有离子键,ClO2中含有极性共价键,Cl2中含有非极性键,故C错误;
D、由三种小球表示的原子及微观过程可知,反应物为氯气和NaClO2,生成物为ClO2和NaCl,则反应为Cl2+2NaClO2═2ClO2+2NaCl,故D正确;
故选D.
B、根据化合价规则,NaClO2和ClO2中Cl的化合价分别是+3价和+4价,化合价不一样,故B错误;
C、该反应涉及的物质含有Cl2、NaClO2、ClO2、NaCl,其中NaClO2、NaCl中均含有离子键,ClO2中含有极性共价键,Cl2中含有非极性键,故C错误;
D、由三种小球表示的原子及微观过程可知,反应物为氯气和NaClO2,生成物为ClO2和NaCl,则反应为Cl2+2NaClO2═2ClO2+2NaCl,故D正确;
故选D.
点评:本题考查氧化还原反应及反应的微观过程的认识,明确反应的分类及常见元素的化合价是解答本题的关键,难度不大,注重了对基础知识的考查.

练习册系列答案
相关题目