题目内容
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某班同学用如下实验探究其性质。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,配制成FeSO4溶液。在溶液中需加入少量铁屑,其目的是_____。
(2)甲组同学取2 mLFeSO4溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeSO4溶液与氯水反应的离子方程式为______。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mLFeSO4溶液中先加入0.5 mL 煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_________。
(4)丙组同学向盛有H2O2溶液的试管中加入几滴酸化的FeSO4溶液,溶液变成棕黄色,发生反应的离子方程式为________________
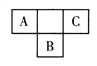
(5)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①仪器B的名称是______。
②将下列实验操作步骤正确排序_____(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=_________(列式表示)。若实验时按a、d次序操作,则使x_______(填“偏大”“偏小”或“无影响”)。
【答案】防止Fe2+被氧化 2Fe2++Cl2=2Fe3++2Cl-隔绝空气(排除氧气对实验的影响)H2O2+2Fe2++2H+=2Fe3++2H2O干燥管dabfce![]() 偏小
偏小
【解析】
(1)配制FeSO4溶液时,需在溶液中加入少量铁屑,防止Fe2+被氧化;(2)氯气具有强氧化性,能将Fe2+氧化为Fe3+,故反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-;(3)为防止空气中的氧气进入,隔绝空气,排除氧气对实验的影响,煤油的作用是隔绝空气;(4)过氧化氢具有强氧化性,能将Fe2+氧化为Fe3+,自身被还原为水,发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O;(5)①根据仪器构造可知仪器B的名称是干燥管;②由于装置中含有空气,空气能氧化硫酸亚铁,所以加热前需要排尽装置中空气,利用氮气排出空气,为了使生成的水蒸气完全排除,应该先熄灭酒精灯,再冷却,然后关闭K1和K2,最后称量,即正确的排序是dabfce;③样品的质量是(m2-m1)g,加热后剩余固体是硫酸亚铁,质量为(m3-m1)g,生成水的质量为(m2-m3)g,
FeSO4·xH2O![]() FeSO4 + xH2O
FeSO4 + xH2O
152 18x
(m3-m1)g (m2-m3)g
则:![]() ,解得:
,解得:![]() ;若实验时按a、d次序操作,在加热过程中部分硫酸亚铁被空气氧化为硫酸铁,导致m3增加,使测得生成的水偏小,生成的硫酸亚铁偏大,因此x偏小。
;若实验时按a、d次序操作,在加热过程中部分硫酸亚铁被空气氧化为硫酸铁,导致m3增加,使测得生成的水偏小,生成的硫酸亚铁偏大,因此x偏小。

【题目】不同温度下,三个体积均为1 L的密闭容器中发生反应3H2(g)+N2(g)![]() 2NH3(g)ΔH =-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表。下列说法正确的是
2NH3(g)ΔH =-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表。下列说法正确的是
容器编号 | 温度(K) | 起始物质的量/mol | 平衡物质的量/mol | ||
H2 | N2 | NH3 | H2 | ||
Ⅰ | T1 | 3 | 1 | 0 | 2.4 |
Ⅱ | T2 | 1.2 | 0.4 | 0.2 | 1.2 |
Ⅲ | T1 | 2 | 0.2 | 0.2 | |
A. T1>T2
B. 平衡时,容器Ⅰ中反应放出的热量为92.6 kJ
C. 容器Ⅰ和容器Ⅱ中反应的化学平衡常数相同
D. 容器Ⅲ中的反应起始时向逆反应方向进行
【题目】T1 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1),下列说法错误的是( )
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1),下列说法错误的是( )
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 2.00 | 3.00 |
t1 | 0.80 | |
t2 | 1.80 |
A. 用H2表示反应在t1 min内的平均速率为v(H2)=0.60/t1mol·L-1·min-1
B. 保持其他条件不变,若起始时向容器中充入3.00 mol CO和2.00 mol H2O(g),达到平衡时,n(CO2)=1.20 mol
C. 保持其他条件不变,在t2 min时向容器中再通入1.00 mol CO,与原平衡相比,达到新平衡时CO转化率将增大
D. 温度升至T2 ℃,上述反应的平衡常数为0.70,则正反应的ΔH<0