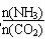��Ŀ����
��Ԫ�ؼ��仯�����ڹ�����ѧ��������������ҪӦ�ã���1��д��ʵ������NH3�Ļ�ѧ��Ӧ����ʽ
��2����ҵ�ϳɰ���ԭ���ǵ����������������Ǵӿ����з�������ģ���������Դ��ˮ��̼�⻯���д������Ȼ��Ϊԭ����ȡ�����Ļ�ѧ��Ӧ����ʽ
��3���ںϳɰ���ԭ�����Ʊ������л���CO�Դ����ж������ã�����ȥԭ�����е�CO����ͨ�����·�Ӧ��ʵ�֣�CO��g��+H2O��g��?CO2��g��+H2��g����H��0����Ӧ�ﵽƽ���Ϊ���CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��
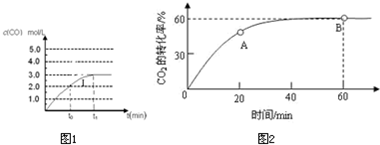
��4�����ݻ�Ϊ2L�����з�����ӦCO��g��+H2O��g��?CO2��g��+H2��g������֪c��CO���뷴Ӧʱ��t�仯���ߢ�����t0ʱ�̽����������������4L������ͼ1�л��c��CO���뷴Ӧʱ��t�仯���ߢ�
��5����ҵ������CO��NH2��2��CO2��NH3��һ�������ºϳɣ��仯ѧ��Ӧ����ʽΪ
��6���ϳ����أ�����̼��
| n(NH3) | n(CO2) |
��A����淴Ӧ����v����CO2��
��NH3��ƽ��ת����Ϊ
��������1�������η�Ӧ�����¼�����Σ����������ɰ�����
��2�����������غ���н��
��3�����CO��ת���ʿ���ʹƽ��������У����ݻ�ѧƽ���ƶ�ԭ�����ش��жϣ�����ƽ�ⳣ��������ʽ�����㣻
��4��CO��g��+H2O��g��?CO2��g��+H2��g������һ��Ӧǰ�������������ķ�Ӧ������2L������t0ʱc��CO��=2.0mol/L����t0ʱ�̽����������������4L����ʱc��CO��=1.0mol/L��ƽ�ⲻ�ƶ�����Ũ��δԭƽ��ʱ��
��
��5��CO2��NH3�ϳ�CO��NH2��2������Ԫ���غ��֪��ͬʱ����H2O���ɣ���ƽ��д����ʽ��
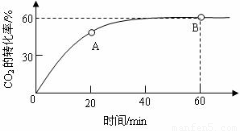
��6������CO2��ת������ʱ��仯ͼ��֪��A��ʱ��Ӧ��δ�ﵽƽ��״̬����Ӧ�Խ�����������У�
����CO2�ij�ʼ���ʵ���Ϊa����NH3�ij�ʼ���ʵ���Ϊ4a����ͼ��֪��CO2��ת����Ϊ60%����ת���Ķ�����̼Ϊ0.6a�����ݷ���ʽ����ת����NH3�����ʵ������ٸ���ת���ʶ�����㣮
��2�����������غ���н��
��3�����CO��ת���ʿ���ʹƽ��������У����ݻ�ѧƽ���ƶ�ԭ�����ش��жϣ�����ƽ�ⳣ��������ʽ�����㣻
��4��CO��g��+H2O��g��?CO2��g��+H2��g������һ��Ӧǰ�������������ķ�Ӧ������2L������t0ʱc��CO��=2.0mol/L����t0ʱ�̽����������������4L����ʱc��CO��=1.0mol/L��ƽ�ⲻ�ƶ�����Ũ��δԭƽ��ʱ��
| 1 |
| 2 |
��5��CO2��NH3�ϳ�CO��NH2��2������Ԫ���غ��֪��ͬʱ����H2O���ɣ���ƽ��д����ʽ��
��6������CO2��ת������ʱ��仯ͼ��֪��A��ʱ��Ӧ��δ�ﵽƽ��״̬����Ӧ�Խ�����������У�
����CO2�ij�ʼ���ʵ���Ϊa����NH3�ij�ʼ���ʵ���Ϊ4a����ͼ��֪��CO2��ת����Ϊ60%����ת���Ķ�����̼Ϊ0.6a�����ݷ���ʽ����ת����NH3�����ʵ������ٸ���ת���ʶ�����㣮
����⣺��1��ʵ�������Ȼ�狀ͼ�ʯ�ҷ�Ӧ��ȡ��������ӦΪ��Ca��OH��2+2NH4Cl
2NH3��+CaCl2+2H2O��
�ʴ�Ϊ��Ca��OH��2+2NH4Cl
2NH3��+CaCl2+2H2O��
��2�������ڸ��¡���������������ˮ������Ӧ������������һ����̼�������̼�����������غ㣬���ɵó�CH4+H2O
CO+3H2 ����CH4+2H2O
CO2+4H2����
�ʴ�Ϊ��CH4+H2O
CO+3H2 ����CH4+2H2O
CO2+4H2����
��3��CO��g��+H2O��g��?CO2��g��+H2��g����H��0��������ӦΪ���ȷ�Ӧ�������¶ȣ���ѧƽ�����ŷ��ȷ���������У������ճ�ȥ������̼��ѧƽ�������ƶ���
��CO����ʼŨ��Ϊxmol��H2O����ʼŨ��Ϊymol����ת����CO����СֵΪ0.9x��
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ x y 0 0
�仯 0.9x 0.9x 0.9x 0.9x
ƽ�� 0.1x y-0.9x 0.9x 0.9x
����ƽ�ⳣ����ʽ��
=0.627��
��ã�
=13.8���ʴ�ֻҪ��ֵ����13.8��ת���ʾͻᳬ��90%��
�ʴ�Ϊ���ʵ������¶Ȼ����ճ�ȥ������̼��13.8��
��4��CO��g��+H2O��g��?CO2��g��+H2��g������һ��Ӧǰ�������������ķ�Ӧ������2L������t0ʱc��CO��=2.0mol/L����t0ʱ�̽����������������4L����ʱc��CO��=1.0mol/L��ƽ�ⲻ�ƶ�����Ũ��δԭƽ��ʱ��
��c��CO���뷴Ӧʱ��t�仯����Ϊ��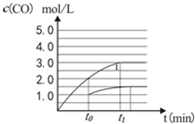 ��
��
�ʴ�Ϊ�� ��
��
��5��CO2��NH3�ϳ�CO��NH2��2������Ԫ���غ��֪��ͬʱ����H2O���ɣ���ѧ����ʽΪ��2NH3+CO2
CO��NH2��2+H2O��
�ʴ�Ϊ���ʴ�Ϊ��2NH3+CO2
CO��NH2��2+H2O��
��6��������CO2��ת������ʱ��仯ͼ��֪��A��ʱ��Ӧ��δ�ﵽƽ��״̬����Ӧ�Խ�����������У���v����CO2��С��B��ƽ��ʱ�Ļ�ѧ��Ӧ���ʣ�
�ʴ�Ϊ������
����CO2�ij�ʼ���ʵ���Ϊa����NH3�ij�ʼ���ʵ���Ϊ4a����ͼ��֪��CO2��ת����Ϊ60%����ת���Ķ�����̼Ϊa��60%=0.6a�����ݷ���ʽ��֪��ת����NH3�����ʵ���Ϊ0.6a��2=1.2a����ƽ��ʱ������ת���ʶ�Ϊ
��100%=30%��
�ʴ�Ϊ��30%��
| ||
�ʴ�Ϊ��Ca��OH��2+2NH4Cl
| ||
��2�������ڸ��¡���������������ˮ������Ӧ������������һ����̼�������̼�����������غ㣬���ɵó�CH4+H2O
| ||
| �� |
| ���� |
| ���� |
�ʴ�Ϊ��CH4+H2O
| ||
| �� |
| ���� |
| ���� |
��3��CO��g��+H2O��g��?CO2��g��+H2��g����H��0��������ӦΪ���ȷ�Ӧ�������¶ȣ���ѧƽ�����ŷ��ȷ���������У������ճ�ȥ������̼��ѧƽ�������ƶ���
��CO����ʼŨ��Ϊxmol��H2O����ʼŨ��Ϊymol����ת����CO����СֵΪ0.9x��
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ x y 0 0
�仯 0.9x 0.9x 0.9x 0.9x
ƽ�� 0.1x y-0.9x 0.9x 0.9x
����ƽ�ⳣ����ʽ��
| (0.9x)2 |
| 0.1x��(y-0.9x) |
��ã�
| y |
| X |
�ʴ�Ϊ���ʵ������¶Ȼ����ճ�ȥ������̼��13.8��
��4��CO��g��+H2O��g��?CO2��g��+H2��g������һ��Ӧǰ�������������ķ�Ӧ������2L������t0ʱc��CO��=2.0mol/L����t0ʱ�̽����������������4L����ʱc��CO��=1.0mol/L��ƽ�ⲻ�ƶ�����Ũ��δԭƽ��ʱ��
| 1 |
| 2 |
 ��
���ʴ�Ϊ��
 ��
����5��CO2��NH3�ϳ�CO��NH2��2������Ԫ���غ��֪��ͬʱ����H2O���ɣ���ѧ����ʽΪ��2NH3+CO2
| ||
�ʴ�Ϊ���ʴ�Ϊ��2NH3+CO2
| ||
��6��������CO2��ת������ʱ��仯ͼ��֪��A��ʱ��Ӧ��δ�ﵽƽ��״̬����Ӧ�Խ�����������У���v����CO2��С��B��ƽ��ʱ�Ļ�ѧ��Ӧ���ʣ�
�ʴ�Ϊ������
����CO2�ij�ʼ���ʵ���Ϊa����NH3�ij�ʼ���ʵ���Ϊ4a����ͼ��֪��CO2��ת����Ϊ60%����ת���Ķ�����̼Ϊa��60%=0.6a�����ݷ���ʽ��֪��ת����NH3�����ʵ���Ϊ0.6a��2=1.2a����ƽ��ʱ������ת���ʶ�Ϊ
| 1.2a |
| 4a |
�ʴ�Ϊ��30%��
�����������Ϊ�ۺϣ��Ӷ���Ƕȿ�����������Ի�ѧƽ���Ӱ�졢��ѧƽ��ͼ��ѧƽ�����ȣ����ؿ��黯ѧƽ���ƶ��ڻ�ѧ�����е�Ӧ���Լ���ѧƽ����㣬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ


 ����
����