题目内容
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示: 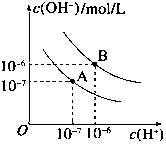
(1)95℃时水的离子积KW=
(2)95℃时,0.01mol/LNaOH溶液的PH= .
(3)95℃时水的电离平衡曲线应为(填“A”或“B”),请说明理由 .
(4)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 .
(5)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 .
(6)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5.请分析原因: .
【答案】
(1)1.0×10﹣12
(2)10
(3)B;水的电离是吸热过程,温度升高电离程度增大,C(H+)、C(OH﹣)均增大
(4)10:1
(5)pH1+pH2=14(或a+b=14)
(6)曲线B对应95℃,此时水的离子积为10﹣12 , HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+,使溶液pH=5
【解析】解:(1)曲线A条件下Kw=c(H+)×c(OH﹣)=10﹣7×10﹣7=10﹣14 , 曲线B条件下c(H+)=c(OH﹣)=10﹣6 mol/L,Kw=c(H+)c(OH﹣)=10﹣12 , 所以答案是:1.0×10﹣12;(2)95℃时,0.01mol/LNaOH溶液中氢氧根离子的浓度为0.01mol/L,所以溶液中氢离子的浓度为:10﹣10mol/L,所以溶液的PH=10,所以答案是:10;(3)95℃时水的电离产生的氢离子和氢氧根离子的浓度相等,所以两者浓度都为10﹣6mol/L,水的电离是吸热过程,温度升高电离程度增大,C(H+)、C(OH﹣)均增大,故选:B;水的电离是吸热过程,温度升高电离程度增大,C(H+)、C(OH﹣)均增大;(4)25℃时所得混合溶液的pH=7,溶液呈中性即酸碱恰好中和,即n(OH﹣)=n(H+),则V(NaOH)10﹣5 molL﹣1=V(H2SO4)10﹣4 molL﹣1 , 得V(NaOH):V(H2SO4)=10:1,所以答案是:10:1;(5)要注意的是95°C时,水的离子积为10﹣12 , 即酸、碱浓度相等时pH(酸)+pH(碱)=12,现强碱的OH﹣浓度是强酸H+浓度的100倍,所以pH(酸)+pH(碱)=14,即pH1+pH2=14,或a+b=14,
所以答案是:pH1+pH2=14(或a+b=14);(6)在曲线B对应温度下,因pH(酸)+pH(碱)=12,可得酸碱两溶液中c(H+)=c(OH﹣),如是强酸碱,两溶液等体积混合后溶液呈中性;现混合溶液的pH=5,即等体积混合后溶液显酸性,说明H+与OH﹣完全反应后又有新的H+产生,酸过量,所以酸HA是弱酸,
所以答案是:曲线B对应95℃,此时水的离子积为10﹣12 , HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+ , 使溶液pH=5.
