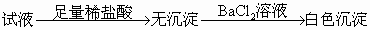题目内容
3位同学设计了下述3个方案,并都认为,如果观察到的现象和自己设计的方案一致,即可确证试液中有方案甲:试液![]() 白色沉淀
白色沉淀![]() 沉淀不溶解
沉淀不溶解
方案乙:试液![]() 无沉淀
无沉淀![]() 溶液白色沉淀
溶液白色沉淀
方案丙:试液足量![]() 无沉淀
无沉淀![]() 溶液白色沉淀
溶液白色沉淀
试评价上述甲、乙、丙三个方案是否严密?并分别简述其理由。
甲方案不够严密,试液中如果没有![]() 而有Ag+,也会有同样的现象变化
而有Ag+,也会有同样的现象变化
乙方案严密,该方案排除了Ag+、![]() 等其他离子的干扰,只有含
等其他离子的干扰,只有含![]() 才可出现该方案中的现象
才可出现该方案中的现象
丙方案不严密,试液中如果没有![]() 而有
而有![]() ,也会有同样的现象变化
,也会有同样的现象变化
解析:方案甲是先加BaCl2溶液,则加入的溶液中含有Ba2+、Cl-,如果试液中含有![]() ,一定出现白色的BaSO4沉淀。加入足量盐酸后,白色沉淀不会消失。若溶液中没有
,一定出现白色的BaSO4沉淀。加入足量盐酸后,白色沉淀不会消失。若溶液中没有![]() ,而有Ag+,则此时也会产生白色AgCl沉淀,且白色沉淀也不会溶于盐酸,所以方案甲是不够严密的。
,而有Ag+,则此时也会产生白色AgCl沉淀,且白色沉淀也不会溶于盐酸,所以方案甲是不够严密的。
方案乙是加入足量盐酸,无沉淀生成,这样就排除了试液中Ag+、Pb2+、Hg2+的存在可能,当再加入BaCl2溶液时,由于产生了白色沉淀,这白色沉淀必然是BaSO4,所以方案乙是严密的。
方案丙是先加入足量稀HNO3,由于稀硝酸具有强的氧化性,倘若试液中无![]() ,而有
,而有![]() 时,则部分
时,则部分![]() 与H+反应生成SO2气体从溶液中逸出;但部分
与H+反应生成SO2气体从溶液中逸出;但部分![]() 在氧化剂稀HNO3的作用下,就氧化成
在氧化剂稀HNO3的作用下,就氧化成![]() ,当再加Ba(NO3)2溶液时,也会产生白色的BaSO4沉淀,这样尽管原试液中没有
,当再加Ba(NO3)2溶液时,也会产生白色的BaSO4沉淀,这样尽管原试液中没有![]() ,也产生了BaSO4沉淀。因此本方案不严密。
,也产生了BaSO4沉淀。因此本方案不严密。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 .试分别说明以下3个方案是否严密?并说明理由.
.试分别说明以下3个方案是否严密?并说明理由.


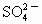 .试分别说明以下3个方案是否严密?并说明理由.
.试分别说明以下3个方案是否严密?并说明理由.