题目内容
下列实验装置(部分仪器已省略)或操作,不能达到相应实验目的是
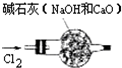
- A.干燥氯气
- B.闻气体气味

- C.分离四氯化碳和水
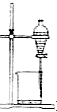
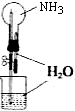
- D.进行喷泉实验
A
分析:A、干燥气体就是除去气体中混有的水蒸气,干燥剂能除去水,但主成分不能与干燥剂反应;
B、根据闻有毒气体的方法:用手在集气瓶口轻轻扇动,仅使极少量的气体飘进鼻孔;
C、根据分液是将不相溶的两种液体分开;
D、根据喷泉实验的条件:气体极易溶于液体或与液体反应,形成内外压强差;
解答:A、干燥气体就是除去气体中混有的水蒸气,碱石灰能除去水,但氢氧化钠也能与氯气反应,所以不能用碱石灰干燥氯气,故A错误;
B、因闻有毒气体的方法:用手在集气瓶口轻轻扇动,仅使极少量的气体飘进鼻孔,故B正确;
C、因分液是将不相溶的两种液体分开,四氯化碳和水是互不相溶的两种液体,可用分液的方法分离,故C正确;
D、因氨气极易溶于水,瓶内压强减小,外压不变,所以形成了喷泉,故D正确;
点评:本题主要考查了常见的实验操作,难度不大,注意知识的积累.
分析:A、干燥气体就是除去气体中混有的水蒸气,干燥剂能除去水,但主成分不能与干燥剂反应;
B、根据闻有毒气体的方法:用手在集气瓶口轻轻扇动,仅使极少量的气体飘进鼻孔;
C、根据分液是将不相溶的两种液体分开;
D、根据喷泉实验的条件:气体极易溶于液体或与液体反应,形成内外压强差;
解答:A、干燥气体就是除去气体中混有的水蒸气,碱石灰能除去水,但氢氧化钠也能与氯气反应,所以不能用碱石灰干燥氯气,故A错误;
B、因闻有毒气体的方法:用手在集气瓶口轻轻扇动,仅使极少量的气体飘进鼻孔,故B正确;
C、因分液是将不相溶的两种液体分开,四氯化碳和水是互不相溶的两种液体,可用分液的方法分离,故C正确;
D、因氨气极易溶于水,瓶内压强减小,外压不变,所以形成了喷泉,故D正确;
点评:本题主要考查了常见的实验操作,难度不大,注意知识的积累.

练习册系列答案
相关题目
利用如图1所示实验装置可以测定一条条件下1mol气体的体积,图1中仪器C称为液体量瓶,瓶颈上有110~130mL刻度线.将一定质量的镁带和过量的衡硫酸在仪器A瓶中完全反应,产生的H2将B瓶中的液体压入液体量瓶中,根据液体的体积可以转换成H2的体积.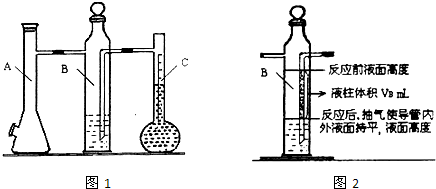
实验步骤:
(1)装配好化学反应气体体积测定仪,作气密性检查.
(2)用砂皮擦去镁带表面的氧化物,然后称取0.100g~0.110g的镁带,把数据记录于表格.
(3)取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口.
(4)用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平.
(5)用注射器吸取10mL 3mol/L硫酸,用针头扎进A瓶加料口橡皮塞,将破酸注入A瓶,注入后迅速拔出针头.
(6)当镁带完全反应后,读取C瓶中液体的体积,把数据记录于表格.
(7)用注射器从A瓶加料口处抽气,使B瓶中导管内外液面持平,记录抽出气体的体积,把数据记录于表格.
重复上述操作进行第二次实验,避免偶然误差.
根据上述实验方法回答下列问题:
实验室温度:25℃,压强:101kPa.该条件下1mol氢气体积的理论值:为24.5L
(1)连接装置及气密性检查:当A瓶加料口塞上橡胶塞, 可以确认装置气密性合格.
(2)B中所装液体一般是 (填“水”或“品红”).A中发生反应的离子方程式为 .
(3)实验数据如下:温度:25℃(镁元素的相对原子质量为24.3)
①上表中X= .
②计算1mol氢气体积两次实验的平均值= L.
③计算实验误差:(实验值-理论值)/理论值×100%= .
④引起该误关的可能原因 (填字母).
A.镁带中含有跟硫酸不反应的杂质
B.没有除去镁带表面的氧化镁
C.镁带中含有杂质铝
D.所用稀硫酸不足量
(4)许多同学在实验中测得的数据偏高(记录数据时已恢复至室温).为此,某化兴趣小组的同学对此实验方案提出了两条修正建议:
①A、B瓶的气体中含有水汽,增加的气体体积中所含的水汽,不该计入氢气的体积.
②B瓶中导管(图2中阴影部分VB)内液柱部分在反应后为空气所占据,不该计入氢气的体积.
你认为他们的意见合理的是 (合理则填序号,否则填“无”).如有合理之处,请根据下面的数据给出修正的1mol氢气体积的数学表达式.(镁元素的相对原子质量为24.3)
1mol氢气体积= L(填写数学表达式).

实验步骤:
(1)装配好化学反应气体体积测定仪,作气密性检查.
(2)用砂皮擦去镁带表面的氧化物,然后称取0.100g~0.110g的镁带,把数据记录于表格.
(3)取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口.
(4)用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平.
(5)用注射器吸取10mL 3mol/L硫酸,用针头扎进A瓶加料口橡皮塞,将破酸注入A瓶,注入后迅速拔出针头.
(6)当镁带完全反应后,读取C瓶中液体的体积,把数据记录于表格.
(7)用注射器从A瓶加料口处抽气,使B瓶中导管内外液面持平,记录抽出气体的体积,把数据记录于表格.
重复上述操作进行第二次实验,避免偶然误差.
根据上述实验方法回答下列问题:
实验室温度:25℃,压强:101kPa.该条件下1mol氢气体积的理论值:为24.5L
(1)连接装置及气密性检查:当A瓶加料口塞上橡胶塞,
(2)B中所装液体一般是
(3)实验数据如下:温度:25℃(镁元素的相对原子质量为24.3)
| 实验次数 | m(Mg)/g | 硫酸体积/mL | 液体量瓶中液体体积/mL | 抽出气体体积/mL | 氢气体积/mL | 计算1mol氢体积/L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | X | |
| 2 | 0.115 | 10.0 | 121.0 | 8.0 |
②计算1mol氢气体积两次实验的平均值=
③计算实验误差:(实验值-理论值)/理论值×100%=
④引起该误关的可能原因
A.镁带中含有跟硫酸不反应的杂质
B.没有除去镁带表面的氧化镁
C.镁带中含有杂质铝
D.所用稀硫酸不足量
(4)许多同学在实验中测得的数据偏高(记录数据时已恢复至室温).为此,某化兴趣小组的同学对此实验方案提出了两条修正建议:
①A、B瓶的气体中含有水汽,增加的气体体积中所含的水汽,不该计入氢气的体积.
②B瓶中导管(图2中阴影部分VB)内液柱部分在反应后为空气所占据,不该计入氢气的体积.
你认为他们的意见合理的是
| 实验次数 | m(Mg) g |
硫酸体积mL | 液体量瓶中液体体积mL | 抽出气体体积mL | B瓶的一段液柱体积mL | 水汽体积百分含量 | 计算1mol氢体积L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | VB | a% |