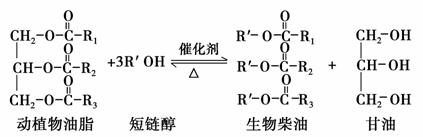
题目内容
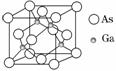 砷化镓广泛用于雷达、电子计算机、人造卫星,宇宙飞船等尖端技术中。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。试回答:
砷化镓广泛用于雷达、电子计算机、人造卫星,宇宙飞船等尖端技术中。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。试回答:
(1)砷化镓的化学式为____________。
(2)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是________(用氢化物分子式表示)。
(3)比较二者的第一电离能:As________(填“<”“>”或“=”)Ga。
(4)下列说法正确的是________(填字母)。
A.砷化镓晶胞结构与NaCl相同
B.砷化镓晶体中与同一个镓原子相连的砷原子构成正四面体
C.电负性:As>Ga
D.砷化镓晶体中含有配位键
解析:由晶胞的结构知每一个砷化镓晶胞中含有4个As原子、4个Ga原子,因此砷化镓的化学式为GaAs。(2)N、P、As为同一主族元素,其氢化物结构相似,相对分子质量越大,则分子间作用力越大,沸点越高,但由于NH3分子间可形成氢键,沸点反常的高,故其氢化物的沸点高低顺序为NH3>AsH3>PH3。(3)As与Ga位于同一周期,分别为ⅤA与ⅢA族,As的p轨道处于半充满的稳定状态,故第一电离能:As>Ga。(4)结合题给GaAs的晶胞结构图可知其晶胞结构与NaCl不同;在GaAs的晶胞中,每个Ga原子连接4个As原子,构成正四面体;结合(3)中分析Ga,As在周期表的位置可知其电负性:As>Ga;在GaAs的晶胞中,每个Ga原子与4个As原子形成4条共价键,由于Ga原子最外层只有3个电子,故其中1条共价键的电子对完全由As原子提供,形成配位键。
答案:(1)GaAs (2)NH3>AsH3>PH3 (3)> (4)BCD

常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,
两种溶液的物质的量浓度和混合溶液的pH如表所示:
| 实验编号 | HA的物质的量浓度(mol·L-1) | NaOH的物质的量浓度(mol·L-1) | 混合后溶 液的pH |
| 甲 | 0.1 | 0.1 | pH=7 |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,判断HA是 (填“强酸”或“弱酸”)
某同学欲利用甲组中的一元酸HA溶液滴定未知浓度的NaOH溶液,可选取 作指示剂;在滴定过程中,下列哪些操作会使结果偏高的是
A.酸式滴定管未用标准酸HA润洗,直接装入标准酸HA
B.酸式滴定管滴定前有气泡,滴定后气泡消失
C.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥
D.读取酸HA体积开始时仰视读数,滴定结束后俯视读数
E.锥形瓶用蒸馏水洗净后,再用待测NaOH溶液润洗
(2)根据乙组数据分析,乙组混合溶液中离子浓度c(A-)和c(Na+)的大小关系是
A.前者大 B.后者大 C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是
(4)分析丁组数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)= mol·L-1。
某同学取丁组试剂各100mL,充分反应后测得放出的热量为Q,写出表示中和热的热化学方程式
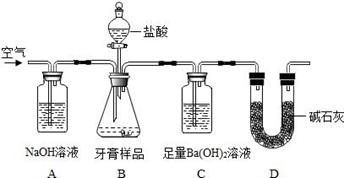
 ________(写化学式)。
________(写化学式)。