题目内容
下列关于四个图像的说法正确的是
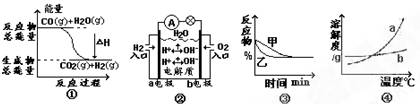
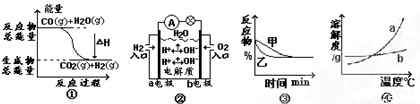
A.图①表示化学反应中能量的变化,反应![]() 的
的![]()
B.图②为氢氧燃料电池示意图,正、负极通入气体体积之比为2:1
C.图③表示压强对可逆反应![]() 的影响,乙的压强大于甲
的影响,乙的压强大于甲
D.图④表示物质a、b的溶解度曲线,可以用结晶方法从a、b混合物中提纯
D
解析:
本题比较综合,考查的知识点有:(1)化学反应中能量变化,(2)燃料电池电极判断及量的计算,(3)平衡图像与平衡移动,(4)溶解度曲线与物质分离提纯的方法。
A错,图①中反应物总能量大于生成物总能量,为放热反应,△H<0。
B错,图②的氢氧燃料电池中电池中b电极O2得电子,b为正极,a电极H2失电子,a为负极,电池总反应方程式为O2+2H2=2H2O,所以正、负极通入气体体积之比为1:2。
C错,由于该可逆反应的产物D的状态为固体,所以反应物的系数大于生成物的系数,若乙的压强大于甲,根据平衡移动原理,加压向气体体积减小的方向移动,该可逆反应将向正反应方向移动,从而使反应物的百分含量减小,不会出现图③中甲、乙的反应物百分含量相同的状况。
D正确,图④中曲线a表示溶解度随温度下降而明显减小的物质(如KNO3),曲线b表示溶解度随温度改变而变化不大的物质(如NaCl),因此利用溶剂对被提纯物质及杂质的溶解度不同,可以使被提纯物质从过饱和溶液中析出,即可通过蒸发结晶或冷却结晶的方式分离提纯。

 名题金卷系列答案
名题金卷系列答案下列关于四个图像的说法正确的是 ( )
|
|


① ②


③ ④
A.图①表示化学反应中能量的变化,反应CO(g)+H2O(g)= CO2(g)+H2(g)的△H>0
B.图②为氢氧燃料电池示意图,正、负极通入的气体体积之比为2︰1
C.图③表示物质a、b的溶解度曲线,可以用结晶方法从a、b 混合物中提纯a
D.图④可以表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,且乙的压强大
3C(g)+D(s)的影响,且乙的压强大
下列关于四个图像的说法正确的是 ( )
 |
A.图①表示化学反应中能量的变化,反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H大于0
B.图②为氢氧燃料电池示意图,正、负极通入气体体积之比为2:1
C.图③表示物质a、b的溶解度曲线,可以用结晶方法从a、b混合物中提纯a
D.图④表示压强对可逆反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
 的
的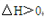
 的影响,乙的压强大于甲
的影响,乙的压强大于甲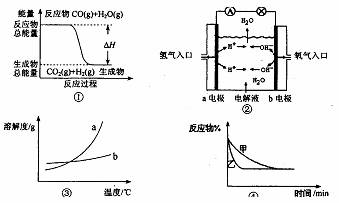
 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大