题目内容
有W、X、Y、Z四种物质,其中两种为单质,两种为化合物,且能发生反应:W+X→Y+Z,则Z不可能是( )
| A、F2 |
| B、Si |
| C、MgO |
| D、Al2O3 |
考点:氯、溴、碘及其化合物的综合应用,硅和二氧化硅,镁、铝的重要化合物
专题:元素及其化合物
分析:两种为单质,两种为化合物,且能发生反应:W+X→Y+Z,说明该反应为置换反应,结合选项中对应物质的性质解答该题.
解答:
解:A.F2性质活泼,氧化性较强,不能用置换的方法制备,故A错误;
B.可为SiO2+2C
2CO+Si,故B正确;
C.可为2Mg+CO2
C+2MgO,故C正确;
D.可为2Al+Fe2O3
2Fe+Al2O3,故D正确.
故选A.
B.可为SiO2+2C
| ||
C.可为2Mg+CO2
| ||
D.可为2Al+Fe2O3
| ||
故选A.
点评:本题综合考查元素化合物知识,为高频考点,侧重于学生的分析能力的考查,注意把握反应的类型以及相关物质的性质的判断,难度不大.

练习册系列答案
相关题目
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色.Q元素的原子最外层电子数是其内层电子数的2倍.W、Z最外层电子数相同,Z的核电荷数是W的2倍.元素Y的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A、原子半径的大小顺序:rX>rY>rW>rQ |
| B、元素Q和Z能形成QZ2型的共价化合物 |
| C、X、Y的最高价氧化物的水化物之间不能反应 |
| D、工业上常用电解的方法制备X、Y的单质 |
下列说法中不正确的是( )
| A、纯净物一定由分子构成 |
| B、由同种分子构成的物质一定是纯净物 |
| C、混合物肯定是由两种以上的元素组成的 |
| D、只含一种元素的物质不一定是纯净物 |
常温下,在溶液中可发生以下反应:①2Fe2++Br2=2Fe3++2Br- ②2Br-+Cl2=Br2+2Cl- ③2Fe3++2I-=2Fe2++I2.由此判断下列说法正确的是( )
| A、铁元素在反应①中被还原,在③中被氧化 |
| B、反应②中当有1mol Cl2被氧化时,有2mol Br-被还原 |
| C、氧化性强弱顺序为:Cl2>I2>Br2>Fe3+ |
| D、还原性强弱顺序为:I->Fe2+>Br->Cl- |
以下有关氨及铵盐的叙述中,不正确的是( )
| A、可以用浓氨水加热制取氨气 |
| B、铵态氮肥不能与碱性物质如草木灰混合施用 |
| C、氨的喷泉实验体现了氨的溶解性和氧化性 |
| D、氨具有还原性,一定条件下可与氧化性的物质如氧气发生反应 |
已知相同条件下,HClO的电离常数小于H2CO3的第一级电离常数(Ka1)大于H2CO3的第二级电离常数(Ka2).为了提高氯水中HClO的浓度,可行的是( )
| A、通入HCl(g) |
| B、加入NaHCO3(s) |
| C、加入H2O |
| D、加入NaOH(s) |
将金属钠分别投入下列物质的水溶液中,产生气体和蓝色沉淀的是( )
| A、NaCl |
| B、K2SO4 |
| C、CuCl2 |
| D、MgCl2 |
关于溶液的下列说法正确的是( )
| A、用湿润的pH试纸测稀碱液的pH,测定值偏大 |
| B、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
| C、已知:H2B?H++HB-,HB-?H++B2-(电离常数K1=1.3×10-7,K2=7.1×10-15),则NaHB溶液显酸性 |
| D、除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
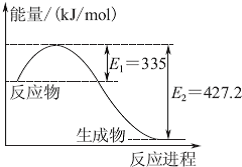 (1)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
(1)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol