题目内容
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
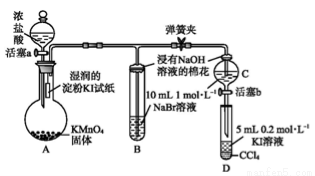
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其化学方程式是 。
(2)验证氯气的氧化性强于碘的实验现象是 。
(3)B中溶液发生反应的离子方程式是 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 。
(5)过程Ⅲ实验的目的是 。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 ,得电子能力逐渐减弱。
(1)16HCl(浓)+2KMnO4=2MnCl2+2KCl+5Cl2↑+8H2O
(2)淀粉KI试纸变蓝
(3)Cl2+2Br-=Br2+2Cl-
(4)打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静置后CCl4层溶液变为紫红色
(5)确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰
(6)原子半径逐渐增大
【解析】(4)应该把C中生成的Br2滴入D中,因为试管底部有CCl4,所以还需振荡静置,观察现象;(5)确认C中没有过量氯气,可以排除Cl2与KI溶液反应。

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案草酸(H2C2O4)是一种弱酸,在工业中有重要作用。某同学查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”,他将菠菜研磨成汁,热水浸泡,经过滤得到溶液,加入足量的CaCl2溶液,产生白色沉淀,过滤、洗涤沉淀备用,然后对生成的沉淀进行探究。
(1)草酸盐溶液呈弱碱性的原因是_____________________________________。
(2)该同学对生成的沉淀进行定性探究。
①提出合理假设。
假设1:只存在CaCO3;
假设2:既存在CaCO3,也存在CaC2O4;
假设3:___________________________________________________________。
②基于假设2,设计实验方案,进行实验。请在下表中写出实验步骤以及预期现象和结论。限选实验试剂:
1 mol·L-1 H2SO4、0.1 mol·L-1盐酸、0.01 mol·L-1 KMnO4溶液、澄清石灰水。
实验步骤 | 预期现象和结论 |
步骤1:取少量沉淀于试管中,加入_________________________________ ________________________________ | _______________________________ _______________________________ 说明沉淀中有CaCO3 |
步骤2:_________________________ ________________________________ | ________________________________ |
(3)基于假设3,另一位同学对生成的沉淀进行定量探究。用稀盐酸溶解生成的沉淀,并加水配制成100 mL溶液。每次准确移取25.00 mL该溶液,用0.010 mol·L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。若菠菜样品的质量为m g,则菠菜中草酸及草酸盐(以C2O42—计)的质量分数为________。