题目内容
3.在含有FeCl3和BaCl2的强酸性溶液中通入足量的SO2有白色沉淀生,由此得出的结论是( )①白色沉淀是BaSO4②白色沉淀是BaSO3③白色沉淀是BaSO3和BaSO4的混合物④FeCl3被SO2还原为FeCl2.| A. | ①③ | B. | ②④ | C. | ②③ | D. | ①④ |
分析 氯化铁具有强的氧化性,在酸性环境下能够氧化二氧化硫生成硫酸根离子,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,硫酸根离子与钡离子发生反应生成硫酸钡沉淀,以此解答该题.
解答 解:氯化铁具有强的氧化性,在酸性环境下能够氧化二氧化硫生成硫酸根离子,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,硫酸根离子与钡离子发生反应生成硫酸钡沉淀,亚硫酸酸性弱于盐酸,与氯化钡不反应,所以不会产生亚硫酸钡沉淀,溶液中三价铁离子全部被还原为二价铁离子,
故选:D.
点评 本题考查了二氧化硫、三价铁离子的性质,为高频考点,明确相关物质的化学性质及发生的反应是解题关键,题目难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目
13.下列实验装置和操作能达到实验目的是( )
| A. | 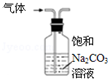 装置可除去CO2中少量的SO2杂质 | B. |  配置一定物质的量浓度的溶液 | ||
| C. | 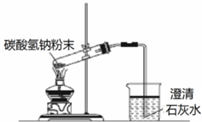 碳酸氢钠受热分解 | D. | 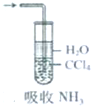 吸收NH3 |
11.有一种信息素的结构简式为CH3(CH2)5CH=CH(CH2)9CHO.下列关于检验该信息素中官能团的试剂和顺序正确的是( )
| A. | 先加入新制氢氧化铜悬浊液,加热;过滤后,调节滤液pH至中性后,在滤液中再加入溴水 | |
| B. | 先加入溴水;后加酸性高锰酸钾溶液 | |
| C. | 先加入酸性高锰酸钾溶液;后加银氨溶液,微热 | |
| D. | 先加入银氨溶液;再另取该物质加入溴水 |
8.将0.4mol/L NH4Cl溶液和0.2mol/L NaOH溶液等体积混合后,溶液中下列微粒的物质的量关系正确的是( )
| A. | c(NH4+)=c(Na+)=c(OH-)>c(NH3•H2O) | B. | c(NH4+)=c(Na+)>c(NH3•H2O)>c(OH-)>c(H+) | ||
| C. | c(NH4+)>c(Na+)>c(OH-)>c(NH3•H2O) | D. | c(NH4+)>c(Na+)>c(NH3•H2O)>c(OH-)>c(H+) |
5.下列热化学方程式或离子方程式中,正确的是( )
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) $?_{500℉、30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | |
| D. | CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应△H=+2×283.0 kJ•mol-1 |