题目内容
水的电离过程为H2O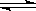 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是
A.C(H+)随着温度升高而降低
B.在35℃时,C(H+)>C(OH-)
C.水的电离度?(25℃)>?(35℃)
D.水的电离是吸热的
【答案】
D
【解析】
试题分析:电离是吸热的,所以升高温度,促进水的电离,氢离子浓度增大,A、C都是不正确的;纯水在任何温度下都是显中性的,B不正确,因此正确的答案选D。
考点:考查水的电离平衡有关判断
点评:本题是基础性试题的考查,试题难易适中,注重基础和能力的双向考查。有利于调动学生的学习积极性和学习兴趣。

练习册系列答案
相关题目