题目内容
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH + HCl =" NaCl" + H2O,
B.2FeCl3 + Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A. B. 。(填“能”或“不能”)
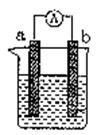
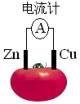
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是 (填“锌”或“铜”),发生 反应(填“氧化”或“还原”);
②正极的电极反应式为 ;
③产生这些气体共需转移电子 mol。
(1)现有如下两个反应:A.NaOH + HCl =" NaCl" + H2O,
B.2FeCl3 + Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A. B. 。(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是 (填“锌”或“铜”),发生 反应(填“氧化”或“还原”);
②正极的电极反应式为 ;
③产生这些气体共需转移电子 mol。
(1)不能 能 .........................................................(2分)
(2)①锌 氧化 .........................................................(2分)
②2H+ +2e- =H2↑ ..........................................................(2分)
③0.3 .........................................................(2分)
略

练习册系列答案
相关题目
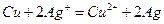

 间后,锌片质量会变小
间后,锌片质量会变小