题目内容
(1)核电荷数小于18的2种元素A、B,A原子最外层电子数为a,次外层电子数为b;B元素原子第3层电子数为a-b,第2层电子数为a+b.则A是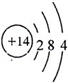
 .
.
(2)某元素的一种同位素原子X的质量数为a,含N个中子,它与H原子组成HmX分子,在b克HmX中所含质子的物质的量是
mol.
(3)已知:碳元素有12C、13C、14C;氧元素有16O、17O、18O,则它们能够形成
O
O
(填元素符号),B的原子结构示意图为

(2)某元素的一种同位素原子X的质量数为a,含N个中子,它与H原子组成HmX分子,在b克HmX中所含质子的物质的量是
| b(m+a-N) |
| m+a |
| b(m+a-N) |
| m+a |
(3)已知:碳元素有12C、13C、14C;氧元素有16O、17O、18O,则它们能够形成
18
18
种CO2分子,它们所形成的CO2分子其相对分子质量有7
7
种.分析:(1)核电荷数小于18的2种元素A、B,A原子最外层电子数为a,次外层电子数为b;B元素原子第3层电子数为a-b,第2层电子数为a+b,则a+b=8,故A有2个电子层,所以b=2,a=8-2=6,所以A为氧元素,B元素原子第3层电子数为a-b=6-2=4,故B为硅元素.
(2)同位素原子X的质量数为a,含N个中子,质子数为a-N,HmX中质子数为m+a-N,b克HmX的物质的量为
mol,据此计算.
(3)碳元素有12C、13C、14C;氧元素有16O、17O、18O,选任意的两种O原子与C原子组合,根据数学组合可知,它们能够形成3×C32种CO2分子,列出可能的CO2分子计算相对分子质量.
(2)同位素原子X的质量数为a,含N个中子,质子数为a-N,HmX中质子数为m+a-N,b克HmX的物质的量为
| b |
| m+a |
(3)碳元素有12C、13C、14C;氧元素有16O、17O、18O,选任意的两种O原子与C原子组合,根据数学组合可知,它们能够形成3×C32种CO2分子,列出可能的CO2分子计算相对分子质量.
解答:解:(1)核电荷数小于18的2种元素A、B,A原子最外层电子数为a,次外层电子数为b;B元素原子第3层电子数为a-b,第2层电子数为a+b,则a+b=8,故A有2个电子层,所以b=2,a=8-2=6,所以A为氧元素,B元素原子第3层电子数为a-b=6-2=4,故B为硅元素,硅原子有3个电子层,最外层电子数为4,原子结构示意图为 .
.
故答案为:O; .
.
(2)同位素原子X的质量数为a,含N个中子,质子数为a-N,HmX中质子数为m+a-N,b克HmX的物质的量为
=
mol,所以含有的质子的物质的量是
mol.
故答案为:
.
(3)碳元素有12C、13C、14C;氧元素有16O、17O、18O,选任意的两种O原子与C原子组合,根据数学组合可知,它们能够形成3×3×(3-1)=18种CO2分子,
由12C、13C、14C、16O、17O、18O组成的CO2分子有:
12C16O2,相对分子质量为12+16×2=44;
12C17O2,相对分子质量为12+17×2=46;
12C18O2,相对分子质量为12+18×2=48;
13C16O2,相对分子质量为13+16×2=45;
13C17O2,相对分子质量为13+17×2=47;
13C18O2,相对分子质量为13+18×2=49;
14C16O2,相对分子质量为14+16×2=46;
14C17O2,相对分子质量为14+17×2=48;
14C18O2,相对分子质量为14+18×2=50;
12C16O17O,相对分子质量为12+16+17=45;
12C16O18O,相对分子质量为12+16+18=46;
12C17O18O,相对分子质量为12+17+18=47;
13C16O17O,相对分子质量为13+16+17=46;
13C16O18O,相对分子质量为13+16+18=47;
13C17O18O,相对分子质量为13+17+18=48;
14C16O17O,相对分子质量为14+16+17=47;
14C16O18O,相对分子质量为14+16+18=48;
14C17O18O,相对分子质量为14+17+18=49;
所以由12C、13C、14C、16O、17O、18O组成的CO2分子的相对分子质量有:44、45、46、47、48、49、50,共7种.
故答案为:18;7.
 .
.故答案为:O;
 .
.(2)同位素原子X的质量数为a,含N个中子,质子数为a-N,HmX中质子数为m+a-N,b克HmX的物质的量为
| bg |
| (m+a)g/mol |
| b |
| m+a |
| b(m+a-N) |
| m+a |
故答案为:
| b(m+a-N) |
| m+a |
(3)碳元素有12C、13C、14C;氧元素有16O、17O、18O,选任意的两种O原子与C原子组合,根据数学组合可知,它们能够形成3×3×(3-1)=18种CO2分子,
由12C、13C、14C、16O、17O、18O组成的CO2分子有:
12C16O2,相对分子质量为12+16×2=44;
12C17O2,相对分子质量为12+17×2=46;
12C18O2,相对分子质量为12+18×2=48;
13C16O2,相对分子质量为13+16×2=45;
13C17O2,相对分子质量为13+17×2=47;
13C18O2,相对分子质量为13+18×2=49;
14C16O2,相对分子质量为14+16×2=46;
14C17O2,相对分子质量为14+17×2=48;
14C18O2,相对分子质量为14+18×2=50;
12C16O17O,相对分子质量为12+16+17=45;
12C16O18O,相对分子质量为12+16+18=46;
12C17O18O,相对分子质量为12+17+18=47;
13C16O17O,相对分子质量为13+16+17=46;
13C16O18O,相对分子质量为13+16+18=47;
13C17O18O,相对分子质量为13+17+18=48;
14C16O17O,相对分子质量为14+16+17=47;
14C16O18O,相对分子质量为14+16+18=48;
14C17O18O,相对分子质量为14+17+18=49;
所以由12C、13C、14C、16O、17O、18O组成的CO2分子的相对分子质量有:44、45、46、47、48、49、50,共7种.
故答案为:18;7.
点评:考查原子结构与位置关系、常用化学用语、常用化学计量计算、同位素、分子的概念、相对分子质量的计算等,比较基础,(3)中关键在于组合出可能的二氧化碳分子.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目