题目内容
【(6分)已知某燃料含碳、氢、氧三种元素,为了测定该燃料的组成:将该燃料放入足量氧气中燃烧,并使产生的CO2和H2O蒸气及剩余的O2全部通过如图所示的装置,得到如下表所列的实验数据(假设生成的气体全部被吸收)。
| | 实验前 | 实验后 |
| 甲的质量 / g | 101.1 | 103.8 |
| 乙的质量 / g | 82.0 | 86.4 |
(1)该燃料分子中碳、氢原子的数目比为 。
(2)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为 。
(6分)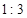 ;C2H6O
;C2H6O
解析试题分析:因为浓硫酸吸收的是水,碱石灰吸收的是二氧化碳,从表格中知道,该燃料燃烧后水是2.7g,二氧化碳是4.4g,物质的量分别为0.15mol、0.1mol,C与H的数目比为1:3;根据式量为46,且每个分子中含有1个氧原子,则含有2个C,6个H,分子式为C2H6O。
考点:烃的燃烧规律及确定分子式的方法。
点评:常见题型,比较简单。

练习册系列答案
相关题目
【(6分)已知某燃料含碳、氢、氧三种元素,为了测定该燃料的组成:将该燃料放入足量氧气中燃烧,并使产生的CO2和H2O蒸气及剩余的O2全部通过如图所示的装置,得到如下表所列的实验数据(假设生成的气体全部被吸收)。

|
|
实验前 |
实验后 |
|
甲的质量 / g |
101.1 |
103.8 |
|
乙的质量 / g |
82.0 |
86.4 |
根据实验数据填空:
(1)该燃料分子中碳、氢原子的数目比为 。
(2)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为 。