题目内容
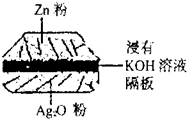
如图:一种微型纽扣电池,其电极材料分别为Ag2O和Zn,电解质溶液是KOH溶液。负极的反应式:Zn-2e-+2OH-==ZnO+H2O,该电池总反应式为:Zn+Ag2O==ZnO+2Ag。
根据以上提供的资料,判断下列说法正确的是
- A.正极的反应式: Ag2O +2e-+H2O=2Ag+2OH-
- B.放电时负极附近溶液的pH不变
- C.放电时每消耗6.5gZn,转移电子0.1mol
- D.放电时溶液中阴离子向正极极方向移动,阳离子向负极方向移动
A
电池总反应式为:Zn+Ag2O==ZnO+2Ag
负极的反应式:Zn-2e-+2OH-==ZnO+H2O
正极的反应式:Ag2O+2e-+H2O ==2Ag+2OH-
B项:由反应式可知,负极反应消耗OH-,故PH减小;
C项:负极式可知,每消耗6.5gZn,转移电子0.2mol
D项:放电时溶液中阴离子向负极方向移动,阳离子向正极方向移动
电池总反应式为:Zn+Ag2O==ZnO+2Ag
负极的反应式:Zn-2e-+2OH-==ZnO+H2O
正极的反应式:Ag2O+2e-+H2O ==2Ag+2OH-
B项:由反应式可知,负极反应消耗OH-,故PH减小;
C项:负极式可知,每消耗6.5gZn,转移电子0.2mol
D项:放电时溶液中阴离子向负极方向移动,阳离子向正极方向移动

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

