题目内容
在一定条件下化学反应:2SO2(g)+O2(g) 2SO3(g);△H=-197 kJ/mol 现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
2SO3(g);△H=-197 kJ/mol 现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
根据以上数据,下列叙述不正确的是
 2SO3(g);△H=-197 kJ/mol 现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
2SO3(g);△H=-197 kJ/mol 现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:| 容器 | SO2(mol) | O2 (mol) | N2 (mol) | Q(kJ) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |
| A.在上述条件下反应生成1 molSO3气体放热98.5 kJ |
| B.2Q2=2Q3<Q1<197 kJ |
| C.Q1=2Q2=2Q3="197" |
| D.在上述条件下每摩该反应进行到底时放出的热量为197 kJ |
C
乙、丙两个容器容积相同,所充气体物质的量相同,丙中所充氮气对平衡无影响。所以乙、丙建立等效平衡,转化率相同,Q1>Q2=Q3,故C错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2SO2+O2,在起始时体积相同的容器A和B中,同时分别充入2molSO3(两容器装有催化剂)。在反应过程中,A保持温度和容积不变;B保持温度和压强不变。回答下列问题:
2SO2+O2,在起始时体积相同的容器A和B中,同时分别充入2molSO3(两容器装有催化剂)。在反应过程中,A保持温度和容积不变;B保持温度和压强不变。回答下列问题: 和1mol
和1mol 充入某固定容积的反应器中,在一定条件下,
充入某固定容积的反应器中,在一定条件下, 达到一定反应限度时有2/3的
达到一定反应限度时有2/3的 转化成
转化成 ,在相同条件下,将1mol
,在相同条件下,将1mol 充入同一反应器中,当反应达到同一反应限度混合气体
充入同一反应器中,当反应达到同一反应限度混合气体 4X(气)+nY(气),反应完全后,容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中n值是
4X(气)+nY(气),反应完全后,容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中n值是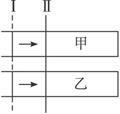
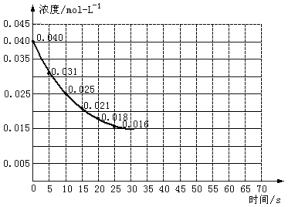
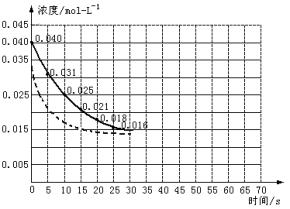
 2C(g)+D(g);△H<0,建立平衡后,保持温度不变,增大加强,建立新平衡时,下列说法错误的是
2C(g)+D(g);△H<0,建立平衡后,保持温度不变,增大加强,建立新平衡时,下列说法错误的是 xC(气)+yD(气),已知起始浓度A为5 mol/L,B为3 mol/L;C的反应速率为0.5 mol/( L·min);反应开始至平衡需2 min;平衡时D的浓度为0.5 mol/L。下列说法不正确的是( )
xC(气)+yD(气),已知起始浓度A为5 mol/L,B为3 mol/L;C的反应速率为0.5 mol/( L·min);反应开始至平衡需2 min;平衡时D的浓度为0.5 mol/L。下列说法不正确的是( ) =2∶1 D. D的反应速率为0.25 mol/(L·min)
=2∶1 D. D的反应速率为0.25 mol/(L·min)