题目内容
.强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq) +OH-(aq)═H2O(l)
△H = -57.3kJ/mol。分别向1L 0.5mol/L的Ba(OH)2的溶液中加入①浓硫酸;② 稀硫酸;③稀硝酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是
△H = -57.3kJ/mol。分别向1L 0.5mol/L的Ba(OH)2的溶液中加入①浓硫酸;② 稀硫酸;③稀硝酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是
| A.△H1<△H2=△H3 | B.△H1>△H2>△H3 |
| C.△H1>△H2=△H3 | D.△H1=△H2<△H3 |
A
试题分析:浓硫酸有强烈的吸水性,溶解于水放出大量的热,所以△H1<△H; 稀硫酸、稀硝酸都电离产生大量的氢离子,在溶液中发生反应H+(aq) +OH-(aq)═H2O(l),放出热量△H2=△H3=△H。所以正确选项为A。

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
 CH3OH(g)过程中的能量变化情况如下图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
CH3OH(g)过程中的能量变化情况如下图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是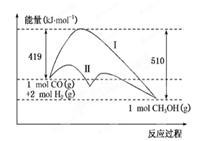
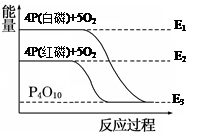
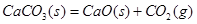 室温下不能自发进行,说明该反应的
室温下不能自发进行,说明该反应的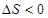
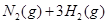


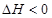 ,其他条件不变时升高温度,反应速率v(H2)和v(NH3)均增大
,其他条件不变时升高温度,反应速率v(H2)和v(NH3)均增大