题目内容
【题目】某同学在实验室研究Fe与H2SO4的反应
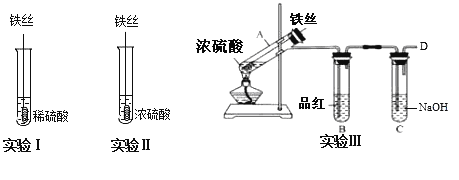
【实验分析】
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为__.
(2)实验Ⅱ中,铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止,
这一现象被称为__.
(3)实验Ⅲ,已知:浓H2SO4的沸点为338.2℃,加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体. A中产生的气体是__,装置C的作用是__.
(4)实验Ⅲ结束后,
甲同学认为装置C中产生Na2SO3,
乙同学认为SO2过量,产物中还可能含有_________,
丙同学认为可能还含有Na2SO4,设计简单实验验证是否含有SO42-,正确的是(____)
A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在
B.先加入硝酸钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在
(5)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性源于+6价的S元素,稀硫酸的氧化性源于________.
②影响反应产物多样性的因素有_____________________(至少填两个).
【答案】 Fe+2H+=Fe2++H2↑ 钝化 SO2 吸收SO2防止污染环境 NaHSO3 C +1价H元素(或H+) 浓度、温度、反应物的量等.
【解析】(1)Fe和稀硫酸反应生成硫酸亚铁和氢气,离子方程式为Fe+2H+=Fe2++H2↑;
(2)浓硫酸具有强氧化性,生成致密的氧化膜覆盖在Fe的表面,发生钝化;
(3)硫酸沸点高、产生气体使品红褪色和D处始终未检测到可燃性气体可推断A中产生的气体为SO2,装置C的作用是吸收SO2防止污染环境;
(4)因Na2SO3+SO2+H2O=2NaHSO3,如果SO2过量,产物中还可能含有NaHSO3;欲检验溶液中含有SO42-,先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在,故答案为C;
(5)①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性表现在+6价的硫元素上,稀硫酸的氧化性表现在+1价的氢(H+)元素上;
②影响反应产物多样性的因素有浓度、温度、反应物的量等。

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案