题目内容
二氯化硫(S2Cl2)是一种琥珀色液体,是合成硫化染料的重要原料。它的熔点-80℃,沸点138℃。常温下,它遇水易反应,产生使品红褪色的气体,且溶液出现浑浊。
(1)写出S2Cl2的电子式_____________________,该分子中Cl—S的键长_______S—S的键长(填“>”,“<”或“=”)。
(2)S2Cl2遇水反应产生气体,该气体分子的空间构型为 ,中心原子的杂化轨道类型为____ 。
(3)HF、H2S、HCl的稳定性由大到小的顺序为 ,沸点由高到低的顺序
为 。
(4)写出二氯化硫与水反应的化学方程式 。
(1)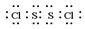 ; < ;(2)V形;sp2;
; < ;(2)V形;sp2;
(3)HF>HCl>H2S ; HF>HCl>H2S ; (4)2S2Cl2+2H2O=SO2 ↑+3S↓+4HCl
解析试题分析:(1)S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,电子式为 ;同周期自左向右原子半径逐渐减小,所以S原子半径大于氯原子半径,故Cl-S的键长<S-S的键长。
;同周期自左向右原子半径逐渐减小,所以S原子半径大于氯原子半径,故Cl-S的键长<S-S的键长。
(2)S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,。根据价层电子对互斥理论可知,S原子的孤对电子对数=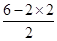 =1,价层电子对数=2+1=3,故二氧化硫为V形,S原子形成sp2杂化。
=1,价层电子对数=2+1=3,故二氧化硫为V形,S原子形成sp2杂化。
(3)非金属性越强,氢化物的稳定性越强。非金属性F>Cl>S,因此氢化物稳定性是HF>HCl>H2S;氟化氢分子之间存在氢键,沸点最高,氯化氢与硫化氢都形成分子晶体,HCl的相对分子质量大,沸点比硫化氢高,故沸点由高到低的顺序为HF>HCl>H2S。
(4)S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),由原子守恒可知还生成水,所以根据电子得失守恒可知反应方程式为2S2Cl2+2H2O=SO2↑+3S↓+4HCl。
考点:考查电子式书写、化学键、分子结构、杂化轨道判断以及元素周期律的应用

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案过氧化氢(H2O2)俗称双氧水,外观为无色透明液体,是一种强氧化剂,适用于伤口及环境、食品消毒;实验室一般用过氧化钡(BaO2)与稀硫酸反应来制取。请问,过氧化钡(BaO2)中所含化学键为
| A.只有离子键 | B.离子键和共价键 |
| C.只有共价键 | D.离子键、共价键和氢键 |
CS2和S2Cl2都是硫的重要化合物,在工业上有广泛的用途。二者的部分性质如下:
| | 熔点/℃ | 沸点/℃ | 密度/g·cm—3[来源 | 水 |
| CS2 | —110.8 | 46.5 | 1.26 | 难溶 |
| S2Cl2 | —76 | 138 | 1.75 | 水解 |
(1)①在 CS2+3Cl2=CCl4(g)+S2Cl2反应中,化合价没发生变化的元素是 。
②在CS2和S2Cl2中,含有非极性键的是 。
(2)以CS2或单质硫做原料与氯气反应都可以制得S2Cl2。下图是实验室里通过在熔融的单质硫中通入少量氯气的方法制取S2Cl2的装置(夹持装置、加热装置均已略去)。
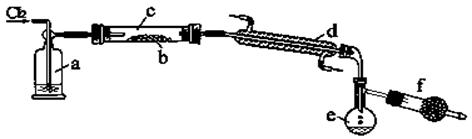
①装置a中的试剂是 ,其作用是 ;
装置d的名称是 ,其作用是 。
②该实验的操作顺序应是 (用序号表示)。
A.加热装置c B.通入Cl2 C.通冷凝水 D.停止通入Cl2
E.停止加热装置c
③f装置中的试剂是 ,其作用是 。
下面有关晶体的叙述中,不正确的是
| A.氯化钠晶体中,每个Na+周围紧邻6个Cl- |
| B.氯化铯晶体中,每个CS+周围紧邻8个Cl- |
| C.氟化钙晶胞中,每个F-周围紧邻8个Ca2+、每个Ca2+周围紧邻8个F- |
| D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |


 键
键