题目内容
阅读以下信息,并回答问题.
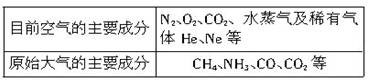
数十亿年来,地球上的物质不断地变化.大气的成分也发生了很大的变化.下表是原始大气和目前空气的主要成分:
用上表所涉及的分子填写下列空白:
(1)由极性键构成的非极性分子有
(2)极易溶于水、其水溶液呈碱性的物质的分子是
(3)分子中不含孤对电子的分子(除稀有气体外)为
(4)CO的结构可表示为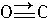 ,与CO结构最相似的分子是
,与CO结构最相似的分子是
(5)随着原始大气中O2的缓慢增加,CH4、NH3、CO等气体逐渐被氧气氧化而缓慢地减少,使大气的成分逐渐演化成目前空气.原始大气中NH3可转化为目前空气中的
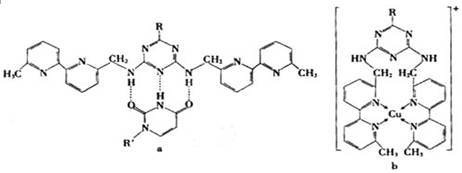
(6)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合或Cu(I)(I表示化合价为+1)时,分别形成a和b:
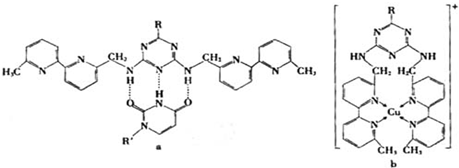
分析a和b中微粒间的相互作用(包括化学键和分子间相互作用),试指出其不同点:
a中含
数十亿年来,地球上的物质不断地变化.大气的成分也发生了很大的变化.下表是原始大气和目前空气的主要成分:
| 目前空气的主要成分 | N2、O2、CO2、水蒸气及稀有气体He、Ne等 |
| 原始大气的主要成分 | CH4、NH3、CO、CO2等 |
(1)由极性键构成的非极性分子有
CH4
CH4
和CO2
CO2
(填写化学式).(2)极易溶于水、其水溶液呈碱性的物质的分子是
NH3
NH3
(填写化学式),它之所以极易溶于水,是因为它的分子和水分子之间可形成氢
氢
键.(3)分子中不含孤对电子的分子(除稀有气体外)为
CH4
CH4
(填写化学式),它的立体构型为正四面体
正四面体
.(4)CO的结构可表示为
 ,与CO结构最相似的分子是
,与CO结构最相似的分子是N2
N2
(填写化学式),这两种结构相似的分子中,分子的极性不相同
不相同
(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫配位
配位
键.(5)随着原始大气中O2的缓慢增加,CH4、NH3、CO等气体逐渐被氧气氧化而缓慢地减少,使大气的成分逐渐演化成目前空气.原始大气中NH3可转化为目前空气中的
N2和H2O
N2和H2O
(填化学式).(6)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合或Cu(I)(I表示化合价为+1)时,分别形成a和b:

分析a和b中微粒间的相互作用(包括化学键和分子间相互作用),试指出其不同点:
a中含
氢键
氢键
,b中含配位键
配位键
.(用“氢键”、“配位键”、“极性键”、“非极性键”等填空)分析:(1)不同非金属元素形成的化学键是极性键,正负电荷重心重合的分子为非极性分子;
(2)氨气极易溶于水,是由于氨气能与水分子之间形成氢键,氨气溶于水,与水反应形成一水合氨,溶液呈碱性;
(3)根据电子式判断CH4中无孤对电子,由于碳原子采取SP3杂化,分子构型为正四面体;
(4)根据等电子体的结构相似来判断;由同种元素组成的双原子分子为非极性分子;由不同种元素组成的双原子分子为极性分子;由CO的结构: 可知分子含有1个配位键,2个共价键;
可知分子含有1个配位键,2个共价键;
(5)根据目前空气的成分以及质量守恒来解答;
(6)根据同种非金属元素之间存在非极性键,不同非金属元素之间存在极性键,含有孤电子对的原子和含有空轨道的原子间存在配位键;氢键应形成于X…H-Y形式当中,X、Y必须是N、O、F元素之一.
(2)氨气极易溶于水,是由于氨气能与水分子之间形成氢键,氨气溶于水,与水反应形成一水合氨,溶液呈碱性;
(3)根据电子式判断CH4中无孤对电子,由于碳原子采取SP3杂化,分子构型为正四面体;
(4)根据等电子体的结构相似来判断;由同种元素组成的双原子分子为非极性分子;由不同种元素组成的双原子分子为极性分子;由CO的结构:
 可知分子含有1个配位键,2个共价键;
可知分子含有1个配位键,2个共价键;(5)根据目前空气的成分以及质量守恒来解答;
(6)根据同种非金属元素之间存在非极性键,不同非金属元素之间存在极性键,含有孤电子对的原子和含有空轨道的原子间存在配位键;氢键应形成于X…H-Y形式当中,X、Y必须是N、O、F元素之一.
解答:解:(1)甲烷中氮原子和氢原子之间存在极性键,甲烷是正四面体结构,正负电荷重心重合;二氧化碳分子中碳原子和氧原子之间存在极性键,二氧化碳是直线型结构,正负电荷重心重合,所以甲烷和二氧化碳是非极性分子,
故答案为:CH4;CO2;
(2)氨气极易溶于水,是由于氨气能与水分子之间形成氢键,氨气溶于水,与水反应形成一水合氨:NH3+H2O?NH3?H2O?NH4++OH-,溶液呈碱性,
故答案为:NH3;氢;
(3)N2、O2、CO2、水蒸气、NH3、CO的孤对电子分别为2对,4对,4对,2对,1对,2对,CH4中无孤对电子,由于碳原子采取SP3杂化,分子构型为正四面体,
故答案为:CH4;正四面体;
(4)CO与N2是等电子体,等电子体的结构相似,N2是由同种元素组成的双原子分子为非极性分子;CO是由不同种元素组成的双原子分子为极性分子;由CO的结构: 可知分子含有1个配位键,2个共价键,
可知分子含有1个配位键,2个共价键,
故答案为:N2;不相同;配位;
(5)目前空气的主要成分N2、O2、CO2、水蒸气,由元素守恒可知原始大气中的NH3转化为现代大气中的N2和H2O,反应方程式为:4NH3+3O2=2N2+6H2O,
故答案为:N2和H2O;
(6)a中碳原子和碳原子之间存在非极性键,碳原子和氮原子之间、氮原子和氢原子之间、碳原子和氢原子之间都存在极性键,氮原子和氢原子之间存在氢键;b中碳原子和碳原子之间存在非极性键,碳原子和氮原子之间、氮原子和氢原子之间、碳原子和氢原子之间都存在极性键,铜原子和氮原子间存在配位键,所以a和b中微粒间的相互作用的不同点:a中含氢键,b中含配位键,
故答案为:氢键;配位键.
故答案为:CH4;CO2;
(2)氨气极易溶于水,是由于氨气能与水分子之间形成氢键,氨气溶于水,与水反应形成一水合氨:NH3+H2O?NH3?H2O?NH4++OH-,溶液呈碱性,
故答案为:NH3;氢;
(3)N2、O2、CO2、水蒸气、NH3、CO的孤对电子分别为2对,4对,4对,2对,1对,2对,CH4中无孤对电子,由于碳原子采取SP3杂化,分子构型为正四面体,
故答案为:CH4;正四面体;
(4)CO与N2是等电子体,等电子体的结构相似,N2是由同种元素组成的双原子分子为非极性分子;CO是由不同种元素组成的双原子分子为极性分子;由CO的结构:
 可知分子含有1个配位键,2个共价键,
可知分子含有1个配位键,2个共价键,故答案为:N2;不相同;配位;
(5)目前空气的主要成分N2、O2、CO2、水蒸气,由元素守恒可知原始大气中的NH3转化为现代大气中的N2和H2O,反应方程式为:4NH3+3O2=2N2+6H2O,
故答案为:N2和H2O;
(6)a中碳原子和碳原子之间存在非极性键,碳原子和氮原子之间、氮原子和氢原子之间、碳原子和氢原子之间都存在极性键,氮原子和氢原子之间存在氢键;b中碳原子和碳原子之间存在非极性键,碳原子和氮原子之间、氮原子和氢原子之间、碳原子和氢原子之间都存在极性键,铜原子和氮原子间存在配位键,所以a和b中微粒间的相互作用的不同点:a中含氢键,b中含配位键,
故答案为:氢键;配位键.
点评:本题考查物质结构和性质,掌握化学键的类型、分子间相互作用是解题的关键,难度中等.

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
| |||||||||||||||
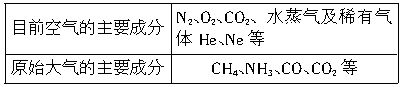
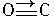 ,与CO结构最相似的分子是________(填写化学式),这两种结构相似的分子中,分子的极性________(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫________键。
,与CO结构最相似的分子是________(填写化学式),这两种结构相似的分子中,分子的极性________(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫________键。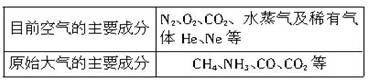


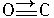 ,与CO结构最相似的分子是________(填写化学式),这两种结构相似的分子中,分子的极性________(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫________键。
,与CO结构最相似的分子是________(填写化学式),这两种结构相似的分子中,分子的极性________(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫________键。