题目内容
 常温下钛的化学活性很小,在较高温度下可与多种物质反应.
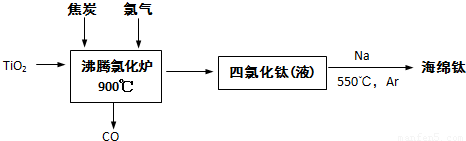
常温下钛的化学活性很小,在较高温度下可与多种物质反应.(1)工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下:

①沸腾氯化炉中发生的主要反应为
TiO2+2C+2Cl2=TiCl4+2CO
TiO2+2C+2Cl2=TiCl4+2CO
.②已知:Ti(s)+2Cl2 (g)═TiCl4(l);△H=a kJ?mol-1
2Na(s)+Cl2(g)═2NaCl(s);△H=b kJ?mol-1
Na(s)═Na(l);△H=c kJ?mol-1
则TiCl4(l)+4Na(l)═Ti(s)+4NaCl(s);△H=
2b-4c-a
2b-4c-a
kJ?mol-1.③TiCl4遇水强烈水解,写出其水解的化学方程式:
TiCl4+4H2O?Ti(OH)4↓+4HCl↑
TiCl4+4H2O?Ti(OH)4↓+4HCl↑
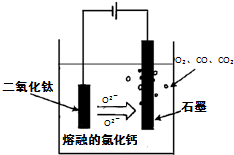
.(2)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如图所示,二氧化钛电极连接电源
负
负
极,该极电极反应为TiO2+4e-=Ti+2O2-
TiO2+4e-=Ti+2O2-
.但此法会产生有毒气体,为减少对环境的污染,在电池中用固体氧离子隔膜(氧离子能顺利通过)将两极产物隔开,再将石墨改为某金属陶瓷电极并通入一种还原性气体,该气体是氢气
氢气
.(3)海绵钛可用碘提纯,原理为Ti(s)+2I2(g)
| >400℃ | 约1250℃ |
CD
CD
(填字母).A.该反应正反应的△H>0
B.在不同温度区域,TiI4的量保持不变
C.在提纯过程中,I2的作用是将粗钛从低温区转移到高温区
D.在提纯过程中,I2可循环利用.
分析:(1)①根据沸腾炉中流程可知反应物为氯气、碳和TiO2,反应生成TiCl4和一氧化碳,依据在守恒配平书写;
②将已知方程式换算成目标方程式,焓变进行相应的改变,结合盖斯定律计算得到;
③水解是结合水电离出的氢氧根离子或氢离子生成弱电解质的过程;
(2)①阴极上得电子发生还原反应;
②阴极上加入的物质应该具有还原性,反应后的生成物没有污染;
(3)(a) 根据反应物和生成物的能量变化确定焓变;
(b) 根据温度判断,在不同温度区域,TiI4的量是否发生改变;
(c) 温度不同,反应方程式不同,产物不同
(d)在提纯过程中,根据反应确定I2的量是否变化;
②将已知方程式换算成目标方程式,焓变进行相应的改变,结合盖斯定律计算得到;
③水解是结合水电离出的氢氧根离子或氢离子生成弱电解质的过程;
(2)①阴极上得电子发生还原反应;
②阴极上加入的物质应该具有还原性,反应后的生成物没有污染;
(3)(a) 根据反应物和生成物的能量变化确定焓变;
(b) 根据温度判断,在不同温度区域,TiI4的量是否发生改变;
(c) 温度不同,反应方程式不同,产物不同
(d)在提纯过程中,根据反应确定I2的量是否变化;
解答:解:(1)沸腾炉中流程可知反应物为氯气、碳和TiO2,反应生成TiCl4和一氧化碳,
反应的化学方程式为:TiO2+2C+2Cl2=TiCl4+2CO;
故答案为:TiO2+2C+2Cl2=TiCl4+2CO;
②(I) Ti(s)+2Cl2(g)=TiCl4(l)△H=a kJ/mol;
(II) 2Na(s)+Cl2(g)=2NaCl(s)△H=bkJ/mol;
(III) Na(s)=Na(l)△H=ckJ/mol,
将方程式2(II)-(I)-4(III)得TiCl4(l)+4Na(l)=Ti(s)+4NaCl(s),△H=2b-4c-a;
故答案为:2b-4c-a;
③TiCl4遇水强烈水解,钛离子结合氢氧根离子形成氢氧化钛出的和氯化氢,反应进行彻底,
反应的化学方程式TiCl4+4H2O?Ti(OH)4↓+4HCl↑;
故答案为:TiCl4+4H2O?Ti(OH)4↓+4HCl↑;
(2)电解时,阴极上得电子发生还原反应,所以二氧化钛得电子生成钛和氧离子,和电源负极相连;电极反应式为TiO2+4e-=Ti+2O2-,阴极上加入的物质应该具有还原性且是气体,反应后的生成物没有污染,水没有污染,所以该气体是氢气,
故答案为:负极;TiO2+4e-=Ti+2O2-;H2;
(3)A、大多数混合反应是放热反应,该反应的正反应也是放热反应,则该反应正反应的△H<0,故A错误;
B、高于400℃,钛和氯气反应生成四氯化钛,在1250℃四氯化钛分解,所以在不同温度区域,TiI4的量不同,故B错误;
C、在提纯过程中,高于400℃,碘和钛反应生成四氯化钛,在1250℃四氯化钛分解生成碘和钛,所以I2的作用是将粗钛从低温区转移到高温区,故C正确;
D、在提纯过程中,高于400℃,碘和钛反应生成四氯化钛,在1250℃四氯化钛分解生成碘和钛,所以I2的量不变,可以循环利用故D正确;
故选CD.
反应的化学方程式为:TiO2+2C+2Cl2=TiCl4+2CO;
故答案为:TiO2+2C+2Cl2=TiCl4+2CO;
②(I) Ti(s)+2Cl2(g)=TiCl4(l)△H=a kJ/mol;
(II) 2Na(s)+Cl2(g)=2NaCl(s)△H=bkJ/mol;
(III) Na(s)=Na(l)△H=ckJ/mol,
将方程式2(II)-(I)-4(III)得TiCl4(l)+4Na(l)=Ti(s)+4NaCl(s),△H=2b-4c-a;
故答案为:2b-4c-a;
③TiCl4遇水强烈水解,钛离子结合氢氧根离子形成氢氧化钛出的和氯化氢,反应进行彻底,
反应的化学方程式TiCl4+4H2O?Ti(OH)4↓+4HCl↑;
故答案为:TiCl4+4H2O?Ti(OH)4↓+4HCl↑;
(2)电解时,阴极上得电子发生还原反应,所以二氧化钛得电子生成钛和氧离子,和电源负极相连;电极反应式为TiO2+4e-=Ti+2O2-,阴极上加入的物质应该具有还原性且是气体,反应后的生成物没有污染,水没有污染,所以该气体是氢气,
故答案为:负极;TiO2+4e-=Ti+2O2-;H2;
(3)A、大多数混合反应是放热反应,该反应的正反应也是放热反应,则该反应正反应的△H<0,故A错误;
B、高于400℃,钛和氯气反应生成四氯化钛,在1250℃四氯化钛分解,所以在不同温度区域,TiI4的量不同,故B错误;
C、在提纯过程中,高于400℃,碘和钛反应生成四氯化钛,在1250℃四氯化钛分解生成碘和钛,所以I2的作用是将粗钛从低温区转移到高温区,故C正确;
D、在提纯过程中,高于400℃,碘和钛反应生成四氯化钛,在1250℃四氯化钛分解生成碘和钛,所以I2的量不变,可以循环利用故D正确;
故选CD.
点评:本题考查了金属的冶炼、电极反应式的书写、热化学反应等知识点,注意焓变的有关计算、电极反应式的书写是高考的热点,应重点掌握.

练习册系列答案
相关题目

 阴极获得钛可能发生的反应或电极反应为:
阴极获得钛可能发生的反应或电极反应为: ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是 。
,下列说法正确的是 。
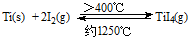
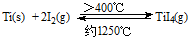 ,下列说法正确的是______.
,下列说法正确的是______.