��Ŀ����
��֪:2CH3OH(g) CH3OCH3(g)+H2O(g) ��H=-25 kJ/mol ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���1 L���ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����£�
CH3OCH3(g)+H2O(g) ��H=-25 kJ/mol ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���1 L���ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����£�

����˵����ȷ����( )
��ƽ��������¶ȣ�ƽ�ⳣ����400
��ƽ��ʱ��c(CH3OCH3)=1.6 mol/L
��ƽ��ʱ����Ӧ����������������20 kJ
��ƽ��ʱ���ټ�������ʼ������CH3OH������ƽ���CH3OHת��������
�ݴ�ʱ�̷�Ӧ�ﵽƽ��״̬
��ƽ��ʱCH3OH��Ũ��Ϊ0.08 mol��L-1
A.�٢ڢܢ� B.�ڢ�
C.�ڢۢܢ� D.�ڢܢ�
B
����������Ϊ����ӦΪ���ȷ�Ӧ�������¶�ƽ�ⳣ����С���ٴ������ݱ������ݿ�֪����Ӧת�����ɵ�CH3OCH3��H2OŨ�Ⱦ�Ϊ1.24 mol��L-1����ʱCH3OH��Ũ��Ϊ0.8 mol��L-1������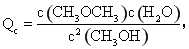 �������ʵ�Ũ�ȴ���ɵã�Qc=2.4��400�����Դ�ʱû�дﵽƽ�⣬��ʱ��Ӧ������Ӧ������У��ݴ����ɻ�ѧƽ�ⳣ�������֪ƽ��ʱc(CH3OCH3)=1.6 mol/L���ڶԣ�����CH3OCH3�����ʵ���Ϊ1.6 mol�����ݷ���ʽ��֪����1.6 mol CH3OCH3�ų�������Ϊ1.6 mol��25 kJ��mol-1=40 kJ���۴���ƽ��ʱ���ټ�������ʼ������CH3OH���൱������ѹǿ��ƽ�ⲻ�ƶ�,CH3OH��ת���ʲ��䣬�ܴ������ݢڿ�֪���ﵽƽ��ʱCH3OH��Ũ��Ϊ0.8 mol��L-1-0.72 mol��L-1=0.08 mol��L-1���ԡ�
�������ʵ�Ũ�ȴ���ɵã�Qc=2.4��400�����Դ�ʱû�дﵽƽ�⣬��ʱ��Ӧ������Ӧ������У��ݴ����ɻ�ѧƽ�ⳣ�������֪ƽ��ʱc(CH3OCH3)=1.6 mol/L���ڶԣ�����CH3OCH3�����ʵ���Ϊ1.6 mol�����ݷ���ʽ��֪����1.6 mol CH3OCH3�ų�������Ϊ1.6 mol��25 kJ��mol-1=40 kJ���۴���ƽ��ʱ���ټ�������ʼ������CH3OH���൱������ѹǿ��ƽ�ⲻ�ƶ�,CH3OH��ת���ʲ��䣬�ܴ������ݢڿ�֪���ﵽƽ��ʱCH3OH��Ũ��Ϊ0.8 mol��L-1-0.72 mol��L-1=0.08 mol��L-1���ԡ�