��Ŀ����
��2009?���ˮ�Ǿ����Դ���⣬�Ӻ�ˮ����ȡʳ�κ���Ĺ������£�
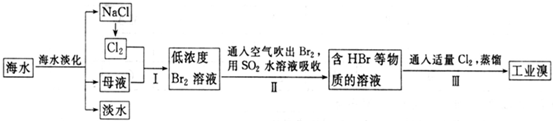
��1�����оٺ�ˮ������һ�ַ�����
��2����NaCl��Һ��⣬�ڵ����п�ֱ�ӵõ��IJ�ƷH2��
��3����������ѻ��Br2����������ֽ�Br2��ԭΪBr-����Ŀ��Ϊ
��4���������SO2ˮ��Һ����Br2�������ʿɴ�95%���йط�Ӧ�����ӷ���ʽΪ
��5��ij��ѧ�о���ѧϰС��Ϊ�˽�ӹ�ҵ�����ᴿ��ķ������������й����ϣ�Br2�ķе�Ϊ59�森����ˮ���ж��Ժ�ǿ��ʴ�ԣ����Dzι��������̺��˽����װ�ã�

�������������ۣ�
��ͼ������B�����ƣ�
������ʵ��װ�����������Ӿ��������������ܣ���ԭ����
��ʵ��װ�����������ã�Ҫ�ﵽ�ᴿ���Ŀ�ģ���������ο��ƹؼ�������
��C��Һ�������ɫΪ

��1�����оٺ�ˮ������һ�ַ�����
�����������������ӽ��������е�һ��
�����������������ӽ��������е�һ��
����2����NaCl��Һ��⣬�ڵ����п�ֱ�ӵõ��IJ�ƷH2��
Cl2
Cl2
��NaOH
NaOH
����H2��NaClO
NaClO
����3����������ѻ��Br2����������ֽ�Br2��ԭΪBr-����Ŀ��Ϊ
������Ԫ��
������Ԫ��
����4���������SO2ˮ��Һ����Br2�������ʿɴ�95%���йط�Ӧ�����ӷ���ʽΪ
SO2+Br2+2H2O�T4H++2Br-+SO42-
SO2+Br2+2H2O�T4H++2Br-+SO42-
���ɴ˷�Ӧ��֪�������������⣬�ڹ�ҵ������Ӧ�������Ҫ������ǿ����豸�����ظ�ʴ
ǿ����豸�����ظ�ʴ
����5��ij��ѧ�о���ѧϰС��Ϊ�˽�ӹ�ҵ�����ᴿ��ķ������������й����ϣ�Br2�ķе�Ϊ59�森����ˮ���ж��Ժ�ǿ��ʴ�ԣ����Dzι��������̺��˽����װ�ã�

�������������ۣ�
��ͼ������B�����ƣ�
������
������
��������ʵ��װ�����������Ӿ��������������ܣ���ԭ����
Br2��ʴ��
Br2��ʴ��
����ʵ��װ�����������ã�Ҫ�ﵽ�ᴿ���Ŀ�ģ���������ο��ƹؼ�������
�����¶ȼ�b���¶ȣ����ռ�59��ʱ�����
�����¶ȼ�b���¶ȣ����ռ�59��ʱ�����
����C��Һ�������ɫΪ
�����ɫ
�����ɫ
��Ϊ��ȥ�ò������Բ���������Cl2���������м���NaBr��Һ����ַ�Ӧ���ٽ��еķ������������
����
����������1����ȥ��ˮ�е��η��Ի�õ�ˮ�Ĺ��չ��̽к�ˮ��������ƺ�ˮ���Σ���ˮ�����ķ����������Ϸ�Ϊ�����ࣺ
�ٴӺ�ˮ��ȡ��ˮ��������������������ˮ������ܼ���ȡ���ͱ�������
�ڳ�ȥ��ˮ�е��η֣��е��������ӽ�������ѹ������
��2����ⱥ���Ȼ�����Һ���������ϲ��������������ϲ���������ͬʱ�������������ƣ����������������������Һ�ɷ�Ӧ���ɴ������ƣ�
��3����ˮ�����õ���ĸҺ�͵���Ȼ�����Һ���ɵ�������Ӧ���õ����嵥��Ũ�ȵͣ��嵥����ˮ����һ�����ܽ����Һ�ˮ��Ӧ����ȡʱ���Ĺ�����Դ��ԭ�ϣ������˾���Ч�棻
��4��SO2�����壬����������ԭ��Ӧ��������д�������ɣ�BrԪ������Ȼ��-1���ȶ������ڴ˷�Ӧ��ǿ��HBr��H2SO4���ɣ���ʴ�豸��˳��д����ҵ������Ҫ��������⣻
��5����ҵ�������ᴿ��ķ�������Ҫ����������������Br2����ǿ�����ԣ��װ���������������ʴ�����Բ����������ܣ���������и�����ϢBr2�ķе���59�棬�ᴿ������ռ�59��ʱ����֣����Կ����¶ȵõ�����ǹؼ���C��Һ��Ϊ���������Ĵ��壬����ɫΪ���غ�ɫ����ȥ�ò������Բ���������Cl2������NaBr��Һ����������Ӧ�����Ȼ��ƺ��嵥�ʣ��ﵽ��ȥ������Ŀ�ģ���ַ�Ӧ��������ķ����õ���
�ٴӺ�ˮ��ȡ��ˮ��������������������ˮ������ܼ���ȡ���ͱ�������
�ڳ�ȥ��ˮ�е��η֣��е��������ӽ�������ѹ������
��2����ⱥ���Ȼ�����Һ���������ϲ��������������ϲ���������ͬʱ�������������ƣ����������������������Һ�ɷ�Ӧ���ɴ������ƣ�
��3����ˮ�����õ���ĸҺ�͵���Ȼ�����Һ���ɵ�������Ӧ���õ����嵥��Ũ�ȵͣ��嵥����ˮ����һ�����ܽ����Һ�ˮ��Ӧ����ȡʱ���Ĺ�����Դ��ԭ�ϣ������˾���Ч�棻
��4��SO2�����壬����������ԭ��Ӧ��������д�������ɣ�BrԪ������Ȼ��-1���ȶ������ڴ˷�Ӧ��ǿ��HBr��H2SO4���ɣ���ʴ�豸��˳��д����ҵ������Ҫ��������⣻
��5����ҵ�������ᴿ��ķ�������Ҫ����������������Br2����ǿ�����ԣ��װ���������������ʴ�����Բ����������ܣ���������и�����ϢBr2�ķе���59�棬�ᴿ������ռ�59��ʱ����֣����Կ����¶ȵõ�����ǹؼ���C��Һ��Ϊ���������Ĵ��壬����ɫΪ���غ�ɫ����ȥ�ò������Բ���������Cl2������NaBr��Һ����������Ӧ�����Ȼ��ƺ��嵥�ʣ��ﵽ��ȥ������Ŀ�ģ���ַ�Ӧ��������ķ����õ���
����⣺��1���Ӻ�ˮ��ȡ��ˮ��������������������ˮ������ܼ���ȡ���ͱ���������ȥ��ˮ�е��η֣��е��������ӽ�������ѹ������
�ʴ�Ϊ�������������������ӽ��������е�һ�֣�
��2�����NaCl��Һ��2NaCl+2H2O
2NaOH+Cl2��+H2������������Cl2ֱ������Һ��NaOH��Ӧ��������������ҺNaClO��
�ʴ�Ϊ��Cl2��NaOH��NaClO��
��3����������ѻ��Br2����������ֽ�Br2��ԭΪBr-��Ŀ���ǵ�Ũ�ȵ�Br2��Һ����ȡʱ���Ĺ����ԭ�Ϻ���Դ��ת��ΪHBr���ױ���������������Ϊ�嵥�ʣ����ڸ�����Ԫ�أ�
�ʴ�Ϊ��������Ԫ�أ�
��4���������������嵥�ʷ�����Ӧ��SO2+Br2+2H2O=H2SO4+2HCI�����ӷ���ʽΪSO2+Br2+2H2O�T4H++2Br-+SO42-������������Ҫ�Ǽ���SO2�������ĺ��ŷţ���ҵ������Ӧ�������Ҫ�����Ƿ�Ӧ����������ǿ�ᣬ��ʴ�豸��
�ʴ�Ϊ��SO2+Br2+2H2O�T4H++2Br-+SO42-��ǿ����豸�����ظ�ʴ��
��5������װ��ͼ��֪���ᴿ�����õ�ԭ������������BΪ�����ܣ��ʴ�Ϊ�������ܣ�
�ڿ����¶�59�棬ʹ�嵥�ʻӷ���ͨ�������õ��������ɫ��Һ̬�嵥�ʣ�ͬʱ������Ⱦ������������β�����գ������嵥����һ��ǿ����������ʴ����Ʒ����������װ�ò������������ܣ��ʴ�Ϊ��Br2��ʴ��
�۴ﵽ�ᴿ���Ŀ�ģ�������Ӧ���ƵĹؼ������ǰ��¶ȿ�������ķе�59��C�����ռ����¶��µ���֣��ʴ�Ϊ�������¶ȼ�b���¶ȣ����ռ�59��ʱ����֣�
�ܸò������Բ���������Cl2������NaBr��Һ������Ӧ��2NaBr+Cl2=2NaCl+Br2�����Գ�ȥ���������ɵ��嵥�ʿ���������ķ����õ����ʴ�Ϊ�������ɫ������
�ʴ�Ϊ�������������������ӽ��������е�һ�֣�
��2�����NaCl��Һ��2NaCl+2H2O
| ||
�ʴ�Ϊ��Cl2��NaOH��NaClO��
��3����������ѻ��Br2����������ֽ�Br2��ԭΪBr-��Ŀ���ǵ�Ũ�ȵ�Br2��Һ����ȡʱ���Ĺ����ԭ�Ϻ���Դ��ת��ΪHBr���ױ���������������Ϊ�嵥�ʣ����ڸ�����Ԫ�أ�
�ʴ�Ϊ��������Ԫ�أ�
��4���������������嵥�ʷ�����Ӧ��SO2+Br2+2H2O=H2SO4+2HCI�����ӷ���ʽΪSO2+Br2+2H2O�T4H++2Br-+SO42-������������Ҫ�Ǽ���SO2�������ĺ��ŷţ���ҵ������Ӧ�������Ҫ�����Ƿ�Ӧ����������ǿ�ᣬ��ʴ�豸��
�ʴ�Ϊ��SO2+Br2+2H2O�T4H++2Br-+SO42-��ǿ����豸�����ظ�ʴ��
��5������װ��ͼ��֪���ᴿ�����õ�ԭ������������BΪ�����ܣ��ʴ�Ϊ�������ܣ�
�ڿ����¶�59�棬ʹ�嵥�ʻӷ���ͨ�������õ��������ɫ��Һ̬�嵥�ʣ�ͬʱ������Ⱦ������������β�����գ������嵥����һ��ǿ����������ʴ����Ʒ����������װ�ò������������ܣ��ʴ�Ϊ��Br2��ʴ��
�۴ﵽ�ᴿ���Ŀ�ģ�������Ӧ���ƵĹؼ������ǰ��¶ȿ�������ķе�59��C�����ռ����¶��µ���֣��ʴ�Ϊ�������¶ȼ�b���¶ȣ����ռ�59��ʱ����֣�
�ܸò������Բ���������Cl2������NaBr��Һ������Ӧ��2NaBr+Cl2=2NaCl+Br2�����Գ�ȥ���������ɵ��嵥�ʿ���������ķ����õ����ʴ�Ϊ�������ɫ������
���������⿼���˺�ˮ��Դ���ۺ����ã���ˮ���幤�գ��ռҵ���̣�ʵ�����������

��ϰ��ϵ�д�
 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д� ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�
�����Ŀ
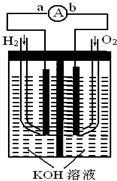 ��2009?�������ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã�
��2009?�������ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã�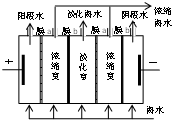 ��2009?����һģ����ˮ��һ����Ļ�ѧ��Դ�⣬�����йغ�ˮ�ۺ����õ�˵����ȷ���ǣ�������
��2009?����һģ����ˮ��һ����Ļ�ѧ��Դ�⣬�����йغ�ˮ�ۺ����õ�˵����ȷ���ǣ�������