题目内容
【题目】下列有关KOH的说法错误的是
A. 是离子化合物 B. 含有共价键
C. 溶于水后离子键会断裂 D. OH-的电子数、质子数均为10
【答案】D
【解析】A. KOH是强碱,属于离子化合物,故A正确;B. KOH中含有氢氧根离子,其中含有共价键,故B正确;C. KOH溶于水发生电离生成钾离子和氢氧根离子,离子键发生断裂,故C正确;D. OH-的电子数为10,质子数为9,故D错误;故选D。

【题目】下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白
族周期 | IA | IIA | IIIA | IV A | V A | VI A | VII A | O |
一 | A | |||||||
二 | B | C | ||||||
三 | D | E | F | G | H | I | ||
四 | K | J | ||||||
(1)这11种元素中化学性质最不活泼的是___,金属性最强的是____.(写元素符号)
(2)第三周期元素中,原子半径最大的元素是(稀有气体元素除外)____,离子半径最小的是____,单质氧化性最强的元素是____.(写元素符号)
(3)J的简单离子的结构示意图__.
(4)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)_____________________.
(5)比较G、H两元素的最高价氧化物对应水化物的酸性____>_____.比较C、G两元素的气态氢化物稳定性____>_____.(写化学式)
(6)C和D的单质在点燃条件下生成化合物的电子式为__,它属于____(离子或共价)化合物.
(7)用电子式表示A和G所形成的简单化合物的形成过程__.
【题目】化石能源的脱硫处理是环保热点问题。
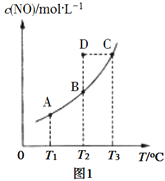
用臭氧处理燃煤烟气脱硫的主要反应如下:![]()
![]() ,向1L反应装置充入
,向1L反应装置充入![]() 和
和![]() ,经过相同反应时间t后剩余
,经过相同反应时间t后剩余![]() 的物质的量与温度关系如图所示:
的物质的量与温度关系如图所示:

已知臭氧会转化成氧气:![]() ,在上述反应条件下臭氧分解率与温度关系如下:
,在上述反应条件下臭氧分解率与温度关系如下:
温度 | 50 | 100 | 150 | 200 | 250 | 300 |
| 0 | 0 | 0 | 4 | 20 | 81 |
![]() 关于脱硫的主要反应,下列说法错误的是______________。
关于脱硫的主要反应,下列说法错误的是______________。
![]() 时,缩小反应装置的体积可以提高相同时间t内
时,缩小反应装置的体积可以提高相同时间t内![]() 的转化率
的转化率
![]() 点该反应处于平衡状态
点该反应处于平衡状态
![]() 随温度的升高,正反应速率变大,逆反应速率减小
随温度的升高,正反应速率变大,逆反应速率减小
![]() 以后随着温度升高,
以后随着温度升高,![]() 的物质的量增多的原因可能是______________________。
的物质的量增多的原因可能是______________________。
![]() 已知
已知![]() 时
时![]() 的平衡常数
的平衡常数![]() ,求该温度下反应
,求该温度下反应![]() 的平衡常数
的平衡常数![]() __________。
__________。
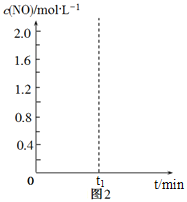
![]() 其他条件不变,经过相同反应时间
其他条件不变,经过相同反应时间![]() ,在图中画出剩余
,在图中画出剩余![]() 的物质的量在
的物质的量在![]() 点温度范围内的关系趋势图____________。
点温度范围内的关系趋势图____________。
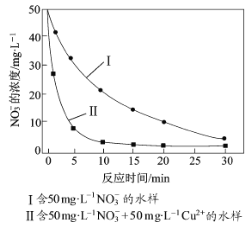
![]() 烟气脱硫后续还需用碱液吸收
烟气脱硫后续还需用碱液吸收![]() 形成
形成![]() ,溶液pH为
,溶液pH为![]() 之间时
之间时![]() 在电解池阴极上被还原成连二硫酸根
在电解池阴极上被还原成连二硫酸根![]() ,写出该电极反应式:___________________________。
,写出该电极反应式:___________________________。