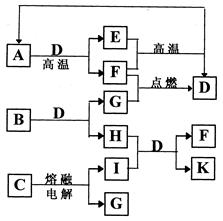
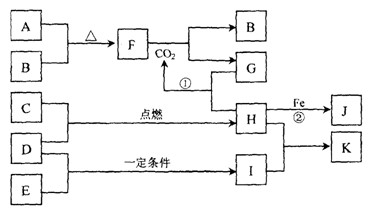
题目内容
下列各组物质的性质比较正确的是( )
| A.碱性:KOH>NaOH>LiOH |
| B.酸性:HNO3>H3PO4>HClO4 |
| C.还原性: Cl->S2->I- |
| D.稳定性:H2O >HF> H2S |
A
金属性越强,最高价氧化物的水化物的碱性越强,A正确。非金属性越强,最高价氧化物的水化物的酸性越强,B中非金属性是Cl>N>P,所以B不正确。非金属性越强,相应阴离子的还原性越弱,C中非金属性是Cl>S>I,C不正确。非金属性越强,相应氢化物的稳定性越强,D中非金属性是F>O>S,D不正确,答案选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
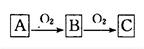
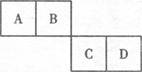
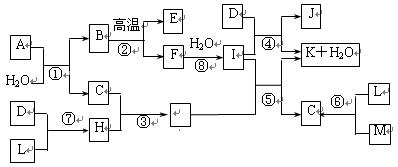
 两容积相等的密闭容器。
两容积相等的密闭容器。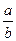 ________
________ 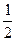 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。