题目内容
1.在密闭容器中,通入x molH2和y mol I2(气),发生反应H2(g)+I2(g)=2HI(g)改变下列条件,反应速率如何改变(填增大、减小或不变)(1)升高温度增大
(2)充入更多的H2增大
(3)扩大容器的体积减小
(4)容器压强不变时,通入氖气减小
(5)容器容积不变时,通入氮气不变
(6)加入正催化剂增大.
分析 增大浓度、增大压强、使用催化剂,反应速率加快,扩大体积,压强减小,速率减小,恒容容器中加入惰气反应速率不变,以此解答该题.
解答 解:(1)升高温度,反应速率增大,故答案为:增大;
(2)再充入H2,反应物浓度增大,化学反应速率增大,故答案为:增大;
(3)将容器容积扩大,相当于减小压强,则反应速率减小,故答案为:减小;
(4)容器压强不变时,通入氖气,为保持恒压,体积增大,反应速率减小,故答案为:减小;
(5)容器容积不变,通入氮气,总压增大分压不变,反应体系中各物质的浓度不变,则反应速率不变,故答案为:不变;
(6)加入正催化剂反应速率增大,故答案为:增大.
点评 本题考查影响化学反应速率的因素,为高频考点,侧重于学生的分析能力的考查,题目较简单,明确常见的影响因素即可解答.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
11.海水是一个巨大的化学资宝库,下列有关海水综合利用的说法,正确的是( )
| A. | 海水中含有氢、氧元素,所以可以使用物理方法从海水中得到氢气 | |
| B. | 从海水中可以得到NaCl,电解NaCl溶液可得到金属钠 | |
| C. | 从海水中提取Br2、I2的过程中发生了氧化还原反应 | |
| D. | 海水蒸发制海盐的过程中只发生了化学变化 |
12.图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述正确的是( )
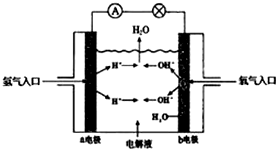

| A. | a电极是正极 | |
| B. | b电极的电极反应为:4OH--4e-=2H2O+O2 | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 氢氧燃料电池是一种具有应用前景的绿色电源 |
9.氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )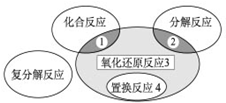

| A. | 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | ||
| C. | CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | D. | Zn+H2SO4═ZnSO4+H2↑ |
16.下列物质属于同系物的一组是( )
| A. | CH4与C2H4 | B. | 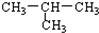 与 CH3-CH2-CH2-CH3 与 CH3-CH2-CH2-CH3 | ||
| C. | C2H6与C3H8 | D. | C2H4与C3H6 |
6.下列叙述正确的是( )
| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 离子化合物中不可能含有共价键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 共价化合物中可能含有离子键 |
13.下列六个图中,横坐标为某溶液中加入某物质的物质的量,纵坐标为生成沉淀的物质的量,请把表中各反应的相应图象的序号填入表中.


| 溶液 | 加入的物质 | 答案序号 |
| 饱和石灰水 | 通过量CO2 | |
| AlCl3溶液 | 通过量NH3 | |
| MgCl2、AlCl3混合溶液 | 逐滴加NaOH溶液至过量 | |
| AlCl3溶液 | 逐滴加NaOH溶液至过量 | |
| 含少量HCl的AlCl3溶液 | 逐滴加NaOH溶液至过量 | |
| FeCl3溶液 | 逐滴加NaOH溶液至过量 |
10.${\;}_1^1H、$${\;}_1^2H、$${\;}_1^3H、$H+、H2,下列说法正确的是( )
| A. | 具有相同的质子数 | B. | 具有不同的电子数 | ||
| C. | 这些微粒互称同位素 | D. | 它们是氢元素不同的五种微粒 |