��Ŀ����
4��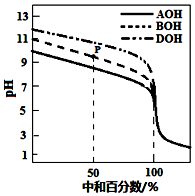 �����£�����ͬ���ʵ���Ũ�ȵ�HCl��Һ���ֱ�ζ����ʵ���Ũ�Ⱦ�Ϊ0.1mol•L-1�����ּAOH��BOH��DOH����Һ���ζ���������ͼ��ʾ�������ж���ȷ���ǣ�������
�����£�����ͬ���ʵ���Ũ�ȵ�HCl��Һ���ֱ�ζ����ʵ���Ũ�Ⱦ�Ϊ0.1mol•L-1�����ּAOH��BOH��DOH����Һ���ζ���������ͼ��ʾ�������ж���ȷ���ǣ�������| A�� | �ζ�ʱ������������Һ�ĵ��룬ˮ�������c��H+��ʼ������ | |
| B�� | �ζ���P��ʱ����Һ�У�c��Cl-����c��B+����c��BOH����c��OH-����c��H+�� | |
| C�� | pH=7ʱ��������Һ��c��Cl-�� ��� | |
| D�� | ���кͰٷ�����100%ʱ����������Һ��Ϻ�c��AOH��+c��BOH��+c��DOH��=c��H+��-c��OH-�� |
���� �����£�����ͬ���ʵ���Ũ�ȵ�HCl��Һ���ֱ�ζ����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L�����ּAOH��BOH��DOH����Һ�����ּ����ʼŨ�Ⱦ�Ϊ0.1mol/L������ͼ���������ʼʱpH����13���������ּ��Ϊ�������ǿ��ΪAOH��BOH��DOH��������ˮ��̶�DCl��BCl��ACl������ˮ��ʹ��Һ�����ԣ������Һ�е��غ�˼�룬�ݴ˷����жϣ�
��� �⣺�����£�����ͬ���ʵ���Ũ�ȵ�HCl��Һ���ֱ�ζ����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L�����ּAOH��BOH��DOH����Һ�����ּ����ʼŨ�Ⱦ�Ϊ0.1mol/L������ͼ���������ʼʱpH����13���������ּ��Ϊ�������ǿ��ΪAOH��BOH��DOH��������ˮ��̶�DCl��BCl��ACl������ˮ��ʹ��Һ�����ԣ�
A���ζ�ʱ������������Һ�ĵ��룬������ͣ����ຬ�������ߣ����������ˮ�ĵ��룬����ˮ��ٽ�ˮ�ĵ��룬��Ӧ�����У�ֻ��˵��ˮ�ĵ���̶Ȳ���������ָˮ�����n��H+��������������ˮ��Ͼ������ģ���Һ���������������ˮ�����c��H+��=$\frac{n��{H}^{+}��}{V}$������Һ�������������n��H+��������������ˮ�������c��H+��ʼ������A����
B���ζ���P��ʱ����ʱ�кͰٷ���Ϊ50%��������Һ����ʼʱǡ�ô���c�����c���Σ�=1��1������P������Ӧ��BOH��Һ��˵����ʼʱǡ��Ϊc��BOH����c��BCl��=1��1����Һ�Լ��ԣ�����BOH����Ϊ����������Һ��c��B+����c��Cl-������B����
C��pH=7ʱ����Һ��c��H+��=c��OH-��������������ˮ��̶Ȳ�һ����DCl��BCl��CCl����ʹ��Һǡ�ó�����ʱ���ζ�DOHʱ����HCl���������Щ��������Һ������HCl��������ȣ���������Һ��c��Cl-���� ��ȣ���C����
D�����кͰٷ�����100%ʱ����������Һ��Ϻ���ʼʱ��Һ��ǡ�ô���c��DCl��=c��BCl��=c��ACl�������������غ㣬c��DOH��+c��AOH��+c��BOH��+c��OH-��=c��H+������c��AOH��+c��BOH��+c��DOH��=c��H+��-c��OH-������D��ȷ��
��ѡD��
���� ������Ҫ�������ζ�ԭ��������ͼ���ж������ּ��Ϊ������ͻ�ƿڣ�ע�������������ˮ�ĵ��룬����ˮ��ٽ�ˮ�ĵ��룬���ΰ�����Һ�е��غ�˼�룬��Ŀ�ѶȲ���

��1����֪����2H2��g��+O2��g��=2H2O��g����H=-483.6kJ/mol
��CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H=+49.0kJ/mol
��д���״�ȼ������H2O��g�����Ȼ�ѧ����ʽCH3OH��g��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��g����H=-676.4kJ/mol��
��2����1L�ܱ������м���2mol CO��4mol H2�����ʵ��Ĵ��������£�������Ӧ��2CO��g��+4H2��g��?CH3OCH3��l��+H2O��l����H=+71kJ/mol
�ٸ÷�Ӧ�ܷ����Է����У���ܡ��������ܡ������жϡ���
������������˵���˷�Ӧ�ﵽƽ��״̬����d��
a����������ƽ����Է����������ֲ��� b��CO��H2��ת�������
c��CO��H2������������ֲ��� d�����������ܶȱ��ֲ���
e��1mol CO���ɵ�ͬʱ��1mol O-H������
��3��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H��0 ��һ�������£�ij��Ӧ�����в������������
| ��Ӧ���� | ��Ӧʱ�� | CO2��mol�� | H2��mol�� | CH3OH��mol�� | H2O��mol�� |
| ���� ���� ��T1�桢 2L�� | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 |
�ڴﵽƽ��ʱ���÷�Ӧ��ƽ�ⳣ��K=$\frac{4}{27}$���÷�����ʾ����ƽ��ʱH2�� ת������50%��
���������������������£���30minʱ�ı��¶�ΪT2�棬��ʱH2�����ʵ���Ϊ3.2mol����T1��T2�����������������=�����������Ǹ÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ���¶����ߣ�ƽ�������ƶ����������������������£���30minʱ���������ٳ���1mol CO2��g����1mol H2O��g������ƽ�ⲻ�ƶ��������������������
��4���ü��ѣ�CH3OCH3����Ϊȼ�ϵ�ص�ԭ�ϣ���д���ڼ��Խ����е�ظ�����ӦʽCH3OCH3-12e-+16OH-=2CO32-+11H2O��
| A�� | c��H+����c��OH-�� | B�� | c��H2C2O4����c��C2O42-�� | ||
| C�� | c��H2C2O4��+c��H+���Tc��C2O42- ��+c��OH-�� | D�� | c��Na+��+c��H+���Tc��HC2O4-��+c��C2O42-��+c��OH-�� |
| A�� | ��ϵ��ѹǿ���ٷ����仯 | |
| B�� | �����ܶȲ��ٷ����仯 | |
| C�� | ����nmol CO��ͬʱ����n mol H2O | |
| D�� | 1 molHһH�����ѵ�ͬʱ����2 mol H-O�� |
| A�� | ���ۺ���ά�����ڶ�������Ȼ�߷��ӻ������һ�������¾���ˮ�� | |
| B�� | ����Ȳ��I2��Na�������Ӵ�������γ�һ�ֵ������ϣ��õ��������й̶����۵� | |
| C�� | ʳ���ͷ������Ȼ�����������������к����� | |
| D�� | ���ع��͡����ӹ��������������Ʒ������������ |
 �ӵ�ʳ���к��е���أ�KIO3�������Ե�ⷨ�Ʊ�����أ�ʵ��װ����ͼ��ʾ���Ƚ�һ�����ĵ����ڹ�������������Һ��������Ӧ��3I2+6KOH=5KI+KIO3+3H2O��������Һ��������������������������Һ��������������ʼ��⣮����˵����ȷ���ǣ�������
�ӵ�ʳ���к��е���أ�KIO3�������Ե�ⷨ�Ʊ�����أ�ʵ��װ����ͼ��ʾ���Ƚ�һ�����ĵ����ڹ�������������Һ��������Ӧ��3I2+6KOH=5KI+KIO3+3H2O��������Һ��������������������������Һ��������������ʼ��⣮����˵����ȷ���ǣ�������| A�� | b�缫�Ǹ��� | |
| B�� | װ���е����ӽ���Ĥ�������ӽ���Ĥ | |
| C�� | �����缫��Ӧ��4OH--4e-�T2H2O+O2�� | |
| D�� | a������KI����ת��ΪKIO3 |
| A�� | �٢ܢݢ� | B�� | �ܢݢ�� | C�� | �ڢݢߢ� | D�� | �ۢܢݢߢ� |
 ������ȥ��Ӧ���������������ж������ɵ��������п��ܵ��ǣ�������
������ȥ��Ӧ���������������ж������ɵ��������п��ܵ��ǣ�������
| A�� | ������ | B�� | ������ | C�� | ������ | D�� | ������ |