题目内容
VL Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量的浓度为
- A.
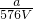 mol/L
mol/L - B.
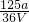 mol/L
mol/L - C.
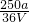 mol/L
mol/L - D.
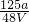 mol/L
mol/L
A
分析:根据n= 计算SO42-的物质的量,进而计算Fe3+的物质的量,根据c=
计算SO42-的物质的量,进而计算Fe3+的物质的量,根据c= 计算Fe3+的物质的量的浓度.
计算Fe3+的物质的量的浓度.
解答:n(SO42-)= =
= mol,则n(Fe3+)=
mol,则n(Fe3+)= ×n(SO42-)=
×n(SO42-)= mol,
mol,
取此溶液0.5VL,n(Fe3+)= mol,
mol,
用水稀释至2VL,则稀释后溶液中Fe3+的物质的量的浓度为:c(Fe3+)= =
=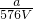 mol/L,
mol/L,
故选A.
点评:本题考查物质的量浓度的计算,题目难度不大,注意硫酸铝的组成,把握相关计算公式.
分析:根据n=
 计算SO42-的物质的量,进而计算Fe3+的物质的量,根据c=
计算SO42-的物质的量,进而计算Fe3+的物质的量,根据c= 计算Fe3+的物质的量的浓度.
计算Fe3+的物质的量的浓度.解答:n(SO42-)=
 =
= mol,则n(Fe3+)=
mol,则n(Fe3+)= ×n(SO42-)=
×n(SO42-)= mol,
mol,取此溶液0.5VL,n(Fe3+)=
 mol,
mol,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量的浓度为:c(Fe3+)=
 =
=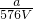 mol/L,
mol/L,故选A.
点评:本题考查物质的量浓度的计算,题目难度不大,注意硫酸铝的组成,把握相关计算公式.

练习册系列答案
相关题目
VL Fe2(SO4)3溶液中含有Fe3+mg,则溶液中SO42-的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
 mol/L
mol/L mol/L
mol/L mol/L
mol/L mol/L
mol/L