题目内容
【题目】合成氨工业中,原料气(N2、H2及CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(l)溶液来吸收原料中的CO,其反应是
[Cu(NH3)2Ac]+CO+NH3![]() [Cu(NH3)3]Ac·CO+Q
[Cu(NH3)3]Ac·CO+Q
(1)必须除去原料气中CO的原因是?
(2)醋酸二氨合铜(l)吸收CO的适宜条件是。
(3)吸收CO后的醋酸铜氨液经过适当处理又可再生,恢复其吸收CO的能力以循环使用,醋酸铜氨液再生的适宜条件是。
【答案】
(1)
CO可引起催化剂中毒
(2)低温、高压
(3)高温、低压
【解析】(1)CO可引起催化剂(铁触媒)的中毒,故要除去。(2)题给信息方程式是一个气体体积减小的放热反应,为使醋酸二氨合铜(l)更好的吸收CO,即平衡向正反应方向移动,适宜条件应是低温、高压。(3)醋酸铜氨液再生,即平衡向逆反应方向移动,适宜的条件应是高温、低压。
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)),还要掌握化学平衡移动原理以及影响因素(影响因素:①浓度:增大反应物(或减小生成物)浓度,平衡向正反应方向移动;②压强:增大压强平衡向气体体积减小的方向移动.减小压强平衡向气体体积增大的方向移动;③温度:升高温度,平衡向吸热反应方向移动.降低温度,平衡向放热反应方向移动;④催化剂:不能影响平衡移动)的相关知识才是答题的关键.

【题目】为了探究外界条件对过氧化氢分解速率的影响,某化学兴趣小组的同学做了以下实验.
编号 | 实验操作 | 实验现象 |
① | 分别在试管A、B中加入5mL5%H2O2溶液,各滴入3滴 | 试管A中不再产生气泡; |
② | 另取两支试管分别加入5mL5%H2O2溶液和5mL10%H2O2 | 两支试管中均未明显见到有 |
请回答下列问题:
(1)过氧化氢分解的化学方程式为 .
(2)实验①的目的是 .
(3)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,你提出的对上述操作的改进意见是(用实验中所提供的几种试剂).
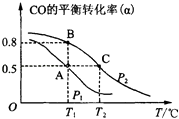
(4)某同学在50mL一定浓度的H2O2溶液中加入适量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图1所示,则A,B,C三点所表示的瞬时反应速率最慢的是(填字母代号). 
(5)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,该兴趣化学小组的同学分别设计了如图2、3所示的实验.请回答相关问题: 
①定性分析:如图2可通过观 , 定性比较得出结论;该实验中将FeCl3溶液改为Fe2(SO4)3溶液的原因是 .
②定量分析:用图3所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略.实验中需要测量的数据是 .
(6)通过对上述实验过程的分析,在实验设计时,要考虑方法的应用.