��Ŀ����
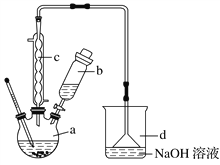
����Ŀ���屽��һ�ֻ���ԭ�ϣ�ʵ���Һϳ��屽��װ��ʾ��ͼ���й��������£�
�� | �� | �屽 | |
�ܶ�/g��cm��3 | 0.88 | 3.10 | 1.50 |
�е�/�� | 80 | 59 | 156 |
ˮ���ܽ�� | �� | �� | �� |
�����кϳɲ���ش����⣺
��1����a�м���15 mL��ˮ����������м����b��С�ļ���4.0 mLҺ̬�塣��a�е��뼸���壬�а�ɫ��������������Ϊ������________���壻�����μ���Һ����ꣻװ��d��������________________��
��2��Һ�����������в�������ᴿ��
����a�м���10 mLˮ��Ȼ����˳�ȥδ��Ӧ����м��
����Һ������10 mLˮ��8 mL 10%��NaOH��Һ��10 mLˮϴ�ӡ�NaOH��Һϴ�ӵ�������_______________________________________________________��
����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����ˡ������Ȼ��Ƶ�Ŀ����____________________________________________ ��
��3�������Ϸ���������屽�л����е���Ҫ����Ϊ______��Ҫ��һ���ᴿ�����в����п��е���________(����ĸ)��
A.�ؽᾧ B.����
C.���� D.��ȡ
��4���ڸ�ʵ���У�a���ݻ����ʺϵ���________(����ĸ)��
A.25 mL B.50 mL
C.250 mL D.500 mL
���𰸡� HBr ����HBr��Br2 ��ȥHBr��δ��Ӧ��Br2 ���� �� C B
��������(1)��м��������a�з����ķ�ӦΪ![]() ��Br2
��Br2![]()
 ��HBr��HBr������ˮ���������������װ��d�������ǽ���β������������HBr�ͻӷ�������������(2)��δ��Ӧ��Br2�������屽�У���Ϊ���ʣ�Br2��ˮ�е��ܽ�Ƚ�С��������NaOH��Һ��Ӧ���ַ�Ӧ���ɵ�HBr��������ˮ���屽����ḽ���������ᣬ��NaOH��Һϴ�ӵ������dz�ȥHBr��δ��Ӧ��Br2�����ֳ��Ĵ��屽�л���ˮ�֣����������Ȼ��ƿ��Գ�ȥˮ�֡�(3)�����屽���ܣ��������������û�г�ȥ�����Լ������Ծ��������������屽�е���Ҫ�����DZ������ݱ����屽�ķе��нϴ���죬������ķ������Խ����߷��롣(4)4.0 mLҺ��ȫ������a�����У���a������Һ������ԼΪ19 mL�����ǵ���ӦʱҺ����ܻ���ڣ�Һ��������ܳ���������
��HBr��HBr������ˮ���������������װ��d�������ǽ���β������������HBr�ͻӷ�������������(2)��δ��Ӧ��Br2�������屽�У���Ϊ���ʣ�Br2��ˮ�е��ܽ�Ƚ�С��������NaOH��Һ��Ӧ���ַ�Ӧ���ɵ�HBr��������ˮ���屽����ḽ���������ᣬ��NaOH��Һϴ�ӵ������dz�ȥHBr��δ��Ӧ��Br2�����ֳ��Ĵ��屽�л���ˮ�֣����������Ȼ��ƿ��Գ�ȥˮ�֡�(3)�����屽���ܣ��������������û�г�ȥ�����Լ������Ծ��������������屽�е���Ҫ�����DZ������ݱ����屽�ķе��нϴ���죬������ķ������Խ����߷��롣(4)4.0 mLҺ��ȫ������a�����У���a������Һ������ԼΪ19 mL�����ǵ���ӦʱҺ����ܻ���ڣ�Һ��������ܳ���������![]() ����ѡ��50 mL����Ϊ�ˡ�
����ѡ��50 mL����Ϊ�ˡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ������������������ꡢ�����ն����⻯ѧ�����Ȼ����������Ҫԭ��֮һ���������������Ⱦ���е��������ѳ�Ϊ���ǹ�ע����Ҫ����֮һ��
I.NH3-SCR���ǹ�ҵ��������������ij��÷������÷������ð��Ļ�ԭ�ԣ���һ�������£��������е�NOxֱ�ӻ�ԭΪN2��
��Ҫ��Ӧԭ��Ϊ��4NH3+4NO+O2![]() 4N2+6H2O
4N2+6H2O
��1����֪�������Ȼ�ѧ����ʽ��
��4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(1) ��H =-1891.5kJmol-1
4N2(g)+6H2O(1) ��H =-1891.5kJmol-1
��N2(g)+O2(g)![]() 2NO(g) ��H =+180.5kJmol-1
2NO(g) ��H =+180.5kJmol-1
��H2O(1)=H2O(g) ��H =+44.0kJmol-1
������������Ӧ����NO����̬ˮ���Ȼ�ѧ����ʽΪ_________________________________��
��2������������ͬ��ij2 L�ܱ������зֱ�Ͷ��2 mol NH3��2 mol NO��1 mol O2���ڼס������ִ��������£�NOת�������¶ȵĹ�ϵ��ͼ��ʾ��
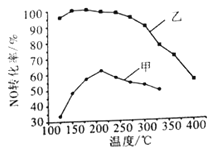
�ٹ�ҵ��ѡ������ҵ�ԭ����_________________��
���ڴ����������£�����210��ʱ��NOת���ʽ��͵�ԭ�������_______________________��
��.CH4�������������������Ⱦ����Ҫ��Ӧԭ��Ϊ��CH4(g)+2NO2(g)= CO2(g)+2H2O(g)+ N2(g) ��H=-868.7kJmol-1
��3����3.00L�ܱ������У�ͨ��0.100mol CH4��0.200mol NO2����һ���¶��½���������Ӧ����Ӧʱ��(t)��������������ѹǿ(P) �����ݼ��±���
��Ӧʱ��t/min | 0 | 2 | 4 | 6 | 8 | 10 |
��ѹǿP/100kPa | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
�ɱ������ݣ�����0-4min��v(NO2)=____________�����¶��µ�ƽ�ⳣ��K=________________��
��4����һ����װ���У�ͨ��һ����CH4��NO2���������ͬʱ���ںͲ�ͬ�¶��£�NO2��ת������(NO2)����ͼ��������������ȷ����_____________
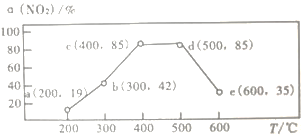
A.���¶�ά����200�����ʱ�䣬NO2��ת���ʽ�����19%
B.��Ӧ���ʣ�b���v(��)>e���v(��)
C.ƽ�ⳣ���� c��=d��
D.��ʱ��t�ڣ����c��ʱNO2��ת���ʺͷ�Ӧ���ʣ����ʵ����»�����c(CH4)
��.��ҵ��Ҳ�����õ��ķ������������������Ⱦ��
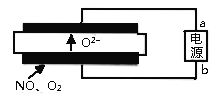
��5���廪��ѧ����������о��Ļ��ڹ������������(SOEC)