题目内容
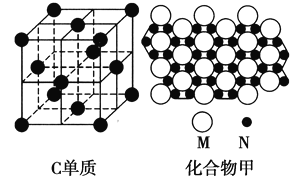
【题目】两种金属元素M和N,其中M单质是人类使用最广泛和最多的金属,N元素的氧化物和氢氧化物均具有两性,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化M可以与一氧化碳发生下列反应:M2O3(s)+3CO(g)![]() 2M(s)+3CO2(g)
2M(s)+3CO2(g)
①元素M名称 ,该反应的平衡常数表达式为:K= 。
②该温度下,在2L盛有M2O3粉末的密闭容器中通入CO气体,10min后,生成了单质M11.2g,则10min内CO的平均反应速率为 。
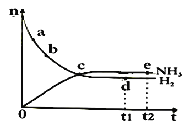
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
① ,
② 。
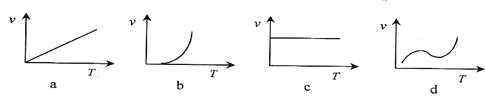
(3)某些金属氧化物粉末和N单质粉末状固体在镁条的引燃下可以发生反应。下列反应速率(v)和温度(T)的关系示意图中与该反应最接近的是 。
(4)写出N的氢氧化物在水中发生碱式电离的电离方程式: ,欲使上述平衡体系中N简单阳离子浓度增加,可加入的物质是 。
【答案】(1)①铁 k=c3(CO2)/c3(CO) ②0.015mol·L-1·min-1
(2)① CO(或CO2)的浓度不再变化
②CO(或CO2)的生成速率消耗速率相等 (其它合理答案均给分)
(3)b(4)Al(OH)3![]() Al3++ 3OH- 盐酸(其它合理答案均给分)
Al3++ 3OH- 盐酸(其它合理答案均给分)
【解析】
试题分析:两种金属元素M和N,其中M单质是人类使用最广泛和最多的金属,N元素的氧化物和氢氧化物均具有两性,则M是铁元素、N是铝元素。(1)在一定温度下:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
①元素M名称铁,固体不写入平衡常数表达式,该反应的平衡常数表达式为:K= c3(CO2)/c3(CO)。
②生成了单质铁11.2g,根据方程式,生成CO2 0.3mol,消耗CO 0.3mol;则10min内CO的平均反应速率为![]() mol·L-1·min-1;(2)根据平衡的定义,① CO(或CO2)的浓度不再变化说明该反应已达到平衡状态;CO(或CO2)的生成速率消耗速率相等,说明该反应已达到平衡状态;(3)温度越高反应速率越快,故b正确;(4)氢氧化铝在水中发生碱式电离的电离方程式:Al(OH)3
mol·L-1·min-1;(2)根据平衡的定义,① CO(或CO2)的浓度不再变化说明该反应已达到平衡状态;CO(或CO2)的生成速率消耗速率相等,说明该反应已达到平衡状态;(3)温度越高反应速率越快,故b正确;(4)氢氧化铝在水中发生碱式电离的电离方程式:Al(OH)3![]() Al3++ 3OH-;欲使铝离子浓度增加,平衡正向移动,可加入的物质是酸,与盐酸、硫酸等。
Al3++ 3OH-;欲使铝离子浓度增加,平衡正向移动,可加入的物质是酸,与盐酸、硫酸等。