题目内容
元素的原子结构决定其性质和在周期表中的位置,下列说法正确的是
A.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
B.某微粒的结构示意简图为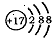 ,则该元素在周期表中位于第三周期、VIA族
,则该元素在周期表中位于第三周期、VIA族
C.Be(OH)2的碱性比Mg(OH)2的碱性强
D.原子半径:Na>Si>O
【答案】
D
【解析】
试题分析:A、元素周期表中位于金属和非金属分界线附近的元素,一般既具有金属性,也具有非金属性,不属于过渡元素。副族和第Ⅷ族元素属于过渡元素,A不正确;
B、某微粒的结构示意简图为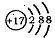 ,则该元素的质子数是17,是氯元素,在周期表中位于第三周期、 ⅦA族,B不正确;
,则该元素的质子数是17,是氯元素,在周期表中位于第三周期、 ⅦA族,B不正确;
C、金属性越强,最高价氧化物的水化物的碱性越强。Be和Mg均是第ⅡA族元素。同主族自上而下金属性逐渐增强,所以Be(OH)2的碱性比Mg(OH)2的碱性弱,C不正确;
D、同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,所以原子半径是Na>Si>O,D正确,答案选D。
考点:考查元素周期表的结构、核外电子排布以及元素周期律的应用等

练习册系列答案
相关题目
元素的原子结构决定其性质和在周期表中的位置.下列说法正确的是( )
| A、所有元素原子的最外层电子数都等于元素的最高化合价 | B、P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 | C、多电子原子中,在离核较近的区域内运动的电子能量较高 | D、元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |