题目内容
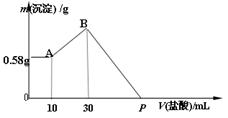
向10mL2mol/L的氯化铝溶液中加入0.5mol/L的烧碱溶液,反应得到沉淀0.78g,则加入的烧碱溶液的体积为
| A.30mL | B.60mL | C.90mL | D.140mL |
BD
氯化铝的物质的量为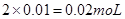 若全部转化为沉淀时生成沉淀的质量为
若全部转化为沉淀时生成沉淀的质量为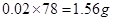 ,此时消耗烧碱的体积是
,此时消耗烧碱的体积是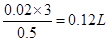 ,为120mL,当氢氧化钠不足时沉淀的质量会小于1.56g,当氢氧化钠溶液的体积大于120mL时,沉淀会发生溶解,导致沉淀质量小于1.56g,当氢氧化钠溶液体积小于120mL时,生成的沉淀时0.78g物质的量为0.01moL,消耗的氢氧化钠的物质的量为0.03moL,此时消耗氢氧化钠溶液的体积是
,为120mL,当氢氧化钠不足时沉淀的质量会小于1.56g,当氢氧化钠溶液的体积大于120mL时,沉淀会发生溶解,导致沉淀质量小于1.56g,当氢氧化钠溶液体积小于120mL时,生成的沉淀时0.78g物质的量为0.01moL,消耗的氢氧化钠的物质的量为0.03moL,此时消耗氢氧化钠溶液的体积是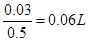 ,即60mL,选B;当氢氧化钠的体积超过120mL时,部分氢氧化钠溶解,根据沉淀的质量可以得出溶解的氢氧化铝的质量是1.56-0.78=0.78g,溶解的氢氧化铝的物质的量是0.01moL,根据反应方程式可知溶解这一部分氢氧化铝消耗的氢氧化钠的物质的量是0.01moL,消耗氢氧化钠溶液的体积是
,即60mL,选B;当氢氧化钠的体积超过120mL时,部分氢氧化钠溶解,根据沉淀的质量可以得出溶解的氢氧化铝的质量是1.56-0.78=0.78g,溶解的氢氧化铝的物质的量是0.01moL,根据反应方程式可知溶解这一部分氢氧化铝消耗的氢氧化钠的物质的量是0.01moL,消耗氢氧化钠溶液的体积是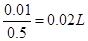 ,为20mL,此过程共消耗氢氧化钠溶液的体积是120+20=140mL,选D,所以答案选BD。
,为20mL,此过程共消耗氢氧化钠溶液的体积是120+20=140mL,选D,所以答案选BD。
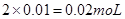 若全部转化为沉淀时生成沉淀的质量为
若全部转化为沉淀时生成沉淀的质量为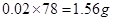 ,此时消耗烧碱的体积是
,此时消耗烧碱的体积是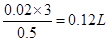 ,为120mL,当氢氧化钠不足时沉淀的质量会小于1.56g,当氢氧化钠溶液的体积大于120mL时,沉淀会发生溶解,导致沉淀质量小于1.56g,当氢氧化钠溶液体积小于120mL时,生成的沉淀时0.78g物质的量为0.01moL,消耗的氢氧化钠的物质的量为0.03moL,此时消耗氢氧化钠溶液的体积是
,为120mL,当氢氧化钠不足时沉淀的质量会小于1.56g,当氢氧化钠溶液的体积大于120mL时,沉淀会发生溶解,导致沉淀质量小于1.56g,当氢氧化钠溶液体积小于120mL时,生成的沉淀时0.78g物质的量为0.01moL,消耗的氢氧化钠的物质的量为0.03moL,此时消耗氢氧化钠溶液的体积是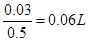 ,即60mL,选B;当氢氧化钠的体积超过120mL时,部分氢氧化钠溶解,根据沉淀的质量可以得出溶解的氢氧化铝的质量是1.56-0.78=0.78g,溶解的氢氧化铝的物质的量是0.01moL,根据反应方程式可知溶解这一部分氢氧化铝消耗的氢氧化钠的物质的量是0.01moL,消耗氢氧化钠溶液的体积是
,即60mL,选B;当氢氧化钠的体积超过120mL时,部分氢氧化钠溶解,根据沉淀的质量可以得出溶解的氢氧化铝的质量是1.56-0.78=0.78g,溶解的氢氧化铝的物质的量是0.01moL,根据反应方程式可知溶解这一部分氢氧化铝消耗的氢氧化钠的物质的量是0.01moL,消耗氢氧化钠溶液的体积是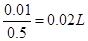 ,为20mL,此过程共消耗氢氧化钠溶液的体积是120+20=140mL,选D,所以答案选BD。
,为20mL,此过程共消耗氢氧化钠溶液的体积是120+20=140mL,选D,所以答案选BD。
练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目