题目内容
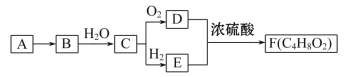
【题目】已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示.

请回答下列问题:
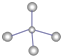
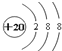
(1)写出A的电子式_______________
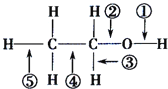
(2)写出②的化学方程式:_____________________________________________
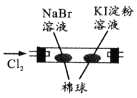
(3)化学课外兴趣小组学生在实验室里制取的A中常混有少量的二氧化硫,老师启发他们设计了如下图实验以确认上述混合气体中有A和SO2.回答下列问题:

①I、II、III、IV装置可盛放的试剂是I______;II______;III______;IV______.(填字母)
A、品红溶液B、NaOH溶液C、浓硫酸D、酸性KMnO4溶液
②使用装置III的目的是______________________________________.
【答案】 ![]() 2CH3CH2OH+O2
2CH3CH2OH+O2![]() 2CH3CHO+2H2O A B A D 检验SO2是否除尽
2CH3CHO+2H2O A B A D 检验SO2是否除尽
【解析】由题中信息可知,A的产量通常用来衡量一个国家的石油化工水平,则A为乙烯;A与水发生加成反应生成B,B为乙醇;B发生催化氧化生成C,C为乙醛;C再发生催化氧化生成D,D为乙酸;B与D发生酯化反应生成E,E为乙酸乙酯。要证明气体中有乙烯和二氧化硫,应先根据二氧化硫的漂白性检验二氧化硫,然后用氢氧化钠溶液除去二氧化硫后再用酸性高锰酸钾溶液检验乙烯。
(1)A为乙烯,其分子中有碳碳双键,其电子式为![]() 。
。
(2)②的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。
(3)①由实验目的可知,I用于检验二氧化硫,通常用品红溶液;II用于吸收二氧化硫,通常用NaOH溶液;III用于检验二氧硫是否除尽,用品红溶液;IV用于检验乙烯,用酸性KMnO4溶液。所以I、II、III、IV装置可盛放的试剂是A、B、A、D.
②使用装置III的目的是检验SO2是否除尽,以免干扰乙烯的检验.

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
装置图 |
|
|
|
|
现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊 |
结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 | Ksp:AgCl>AgBr>AgI | 非金属性:C>Si |
A. AB. BC. CD. D