题目内容
某金属单质能与足量浓硝酸反应,放出NO2气体,若参加反应的金属单质与硝酸的物质的量之比为1:a,则该金属元素在反应后生成的硝酸盐中的化合价是 ( )
A.+2a B.+a C.+a/2 D.+a/4
【答案】
C
【解析】
试题分析:设该金属元素的化合价是+n价,如果金属的物质的量是1mol,则没有被还原的硝酸是nmol,所以被还原的硝酸是(a-n)mol,则根据电子的得失守恒可知,n=a-n,解得n=0.5a,答案选C。
考点:考查金属和硝酸反应的有关计算
点评:该题是高考中的常见考点,属于中等难度的试题。该题的解题思路是根据氧化还原反应中得失的得失守恒进行,本题有利于培养学生分析问题、解决问题的能力,有利于调动学生的学习积极性。

练习册系列答案
相关题目
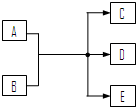
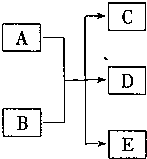 (2010?东城区二模)一定条件下,物质A~E转化关系如右图,其中A为单质,常温下E为无色溶液体.
(2010?东城区二模)一定条件下,物质A~E转化关系如右图,其中A为单质,常温下E为无色溶液体.